题目内容
(1)铜绿的化学式是Cu2(OH)2CO3,它受热会分解生成三种氧化物.铜绿分解的化学方程式为
(2)据铜绿的组成判断,铜“生锈”可能是铜与氧气及
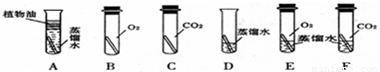
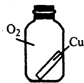
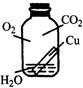
(3)借鉴课本“铁钉锈蚀条件的探究”实验,小梁设计了“铜片锈蚀条件的探究”实验,实验如图所示(所用铜片洁净、光亮,试管内的“ ”为铜片):
”为铜片):
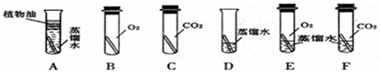
实验较长时间后,发现
Cu2(OH)2CO3
2CuO+H2O+CO2↑
| ||
Cu2(OH)2CO3
2CuO+H2O+CO2↑
.
| ||
(2)据铜绿的组成判断,铜“生锈”可能是铜与氧气及
水和二氧化碳
水和二氧化碳
作用的结果.(3)借鉴课本“铁钉锈蚀条件的探究”实验,小梁设计了“铜片锈蚀条件的探究”实验,实验如图所示(所用铜片洁净、光亮,试管内的“
 ”为铜片):
”为铜片):
实验较长时间后,发现
D
D
试管中铜片最先生锈(填试管字母编号).小区认为小梁设计的实验还不够完善,要得出正确的结论,还要补充一个实验.你认为要补充的一个实验是(用图表示)把铜片置于装有干燥空气的试管中,放置对比观察.
把铜片置于装有干燥空气的试管中,放置对比观察.
.分析:(1)根据反应物和生成物及其质量守恒定律可以书写化学方程式;
(2)根据铜绿的组成判断铜生锈的条件;
(3)比较铜制品生锈的难易要注意所处的环境条件.
(2)根据铜绿的组成判断铜生锈的条件;
(3)比较铜制品生锈的难易要注意所处的环境条件.
解答:解:(1)铜绿受热会分解生成三种氧化物,由黑色粉末可知是氧化铜,其余两种由质量守恒定律知剩余两种应是水和二氧化碳,铜绿分解的化学方程式为:Cu2(OH)2CO3
2CuO+H2O+CO2↑.
故答案为:Cu2(OH)2CO3
2CuO+H2O+CO2↑.
(2)据铜绿的组成和查阅的资料判断,铜绿可能是铜与氧气及水、二氧化碳共同作用而形成的.
故答案为:水和二氧化碳.
(3)实验较长时间后,发现D试管中铜片最先生锈,因为D试管中的铜与氧气、水和二氧化碳充分接触,容易生锈;上图知实验缺少了把铜片置于装有干燥空气(或氧气和二氧化碳)的试管中,所以要补充的一个实验是:把铜片置于装有干燥空气的试管中,放置对比观察.
故答案为:D;把铜片置于装有干燥空气的试管中,放置对比观察.
| ||
故答案为:Cu2(OH)2CO3
| ||
(2)据铜绿的组成和查阅的资料判断,铜绿可能是铜与氧气及水、二氧化碳共同作用而形成的.
故答案为:水和二氧化碳.
(3)实验较长时间后,发现D试管中铜片最先生锈,因为D试管中的铜与氧气、水和二氧化碳充分接触,容易生锈;上图知实验缺少了把铜片置于装有干燥空气(或氧气和二氧化碳)的试管中,所以要补充的一个实验是:把铜片置于装有干燥空气的试管中,放置对比观察.
故答案为:D;把铜片置于装有干燥空气的试管中,放置对比观察.
点评:掌握质量守恒定律,学会对比实验的设计和应用,记住:对比实验一般采用“单一变量原则”,也就是说其他条件不变,只改变一个条件,这样产生的不同结果就是这个因素引起的.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
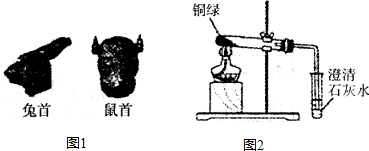 2009年2月12日,我外交部就法国某公司拍卖我国两件重要文物兔首和鼠首(见图1),发表严正声明:中国对其拥有不可置疑的所有权.目前我国正在积极追讨这两件文物.兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿).为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究:
2009年2月12日,我外交部就法国某公司拍卖我国两件重要文物兔首和鼠首(见图1),发表严正声明:中国对其拥有不可置疑的所有权.目前我国正在积极追讨这两件文物.兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿).为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究: ”为铜片):
”为铜片):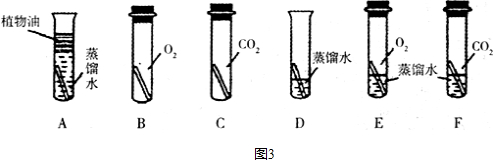



 ”为铜片):
”为铜片):
 ”为铜片):
”为铜片):