��Ŀ����
ijͬѧ�ڲ�������ʱ��֪�����۴�����Ʒ�������Ȼ������ʡ�
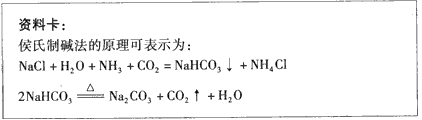
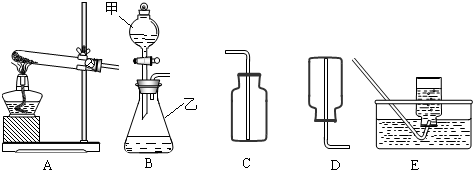
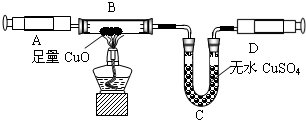
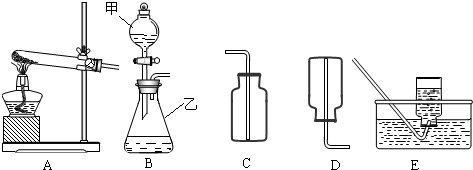
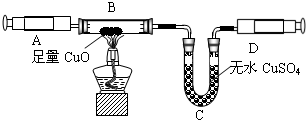
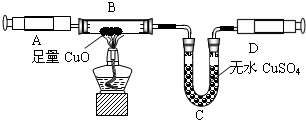
��ͬѧ���������ͼ�е�װ�ý���ʵ�飬�ⶨ���۴�����Ʒ��̼���Ƶ�������������ˮ������Ӱ����Բ��ƣ��г�װ������ȥ��
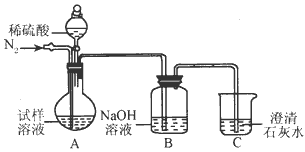
��Ҫʵ�鲽�����£�
�ٰ�ͼ��װ�����������װ�õ������ԣ�
�ڳ���5.5 g���۴�����Ʒ������ƿ�У�����������ˮ�ܽ⣬�õ�������Һ��
�۴ӷ�Һ©���е���ϡ���ᣬֱ�� ���ٲ�������ʱΪֹ��
�ܻ�������һ������N2��
�ݳ���Bƿ����Һ����������������2.2 g�� ��ش��������⣺
(1)д��A�з�����Ӧ�Ļ�ѧ����ʽ_____________ ��
(2)����һ������N2��Ŀ����______________ ��װ��C�г���ʯ��ˮ��������______________ ��
(3)�������Һ©���е�ϡ���ỻ��Ũ���ᣬ���ԵĽ�� ___________�����ƫ�ߡ�����ƫ�͡� ���䡱��
(4)����Ʒ��̼���Ƶ���������Ϊ______________ �������������С�����һλ��
(5)����������ʵ�鷴Ӧԭ����ͬ��ʵ�����ⶨ������Ʒ��̼���Ƶ��������������û�ѧ����ʽ��ʾ��ʵ��ԭ��____________ ��
�ٰ�ͼ��װ�����������װ�õ������ԣ�
�ڳ���5.5 g���۴�����Ʒ������ƿ�У�����������ˮ�ܽ⣬�õ�������Һ��
�۴ӷ�Һ©���е���ϡ���ᣬֱ�� ���ٲ�������ʱΪֹ��
�ܻ�������һ������N2��
�ݳ���Bƿ����Һ����������������2.2 g�� ��ش��������⣺
(1)д��A�з�����Ӧ�Ļ�ѧ����ʽ_____________ ��
(2)����һ������N2��Ŀ����______________ ��װ��C�г���ʯ��ˮ��������______________ ��
(3)�������Һ©���е�ϡ���ỻ��Ũ���ᣬ���ԵĽ�� ___________�����ƫ�ߡ�����ƫ�͡� ���䡱��
(4)����Ʒ��̼���Ƶ���������Ϊ______________ �������������С�����һλ��
(5)����������ʵ�鷴Ӧԭ����ͬ��ʵ�����ⶨ������Ʒ��̼���Ƶ��������������û�ѧ����ʽ��ʾ��ʵ��ԭ��____________ ��
(1) Na2CO3+ H2SO4 ==Na2SO4+ H2O+CO2 ��
(2)�ų�װ��A�������в���CO2��ʹ��ȫ����װ��B��NaOH��Һ���գ� ����CO2�Ƿ�Bƿ�е�NaOH��Һ��ȫ����
(3)ƫ��
(4)96.4%
(5)Na2CO3 +CaCl2==CaCO3 ��+2NaCl(����BaCl2�� Ba(OH)2��Ӧ��
(2)�ų�װ��A�������в���CO2��ʹ��ȫ����װ��B��NaOH��Һ���գ� ����CO2�Ƿ�Bƿ�е�NaOH��Һ��ȫ����
(3)ƫ��
(4)96.4%
(5)Na2CO3 +CaCl2==CaCO3 ��+2NaCl(����BaCl2�� Ba(OH)2��Ӧ��

��ϰ��ϵ�д�
�����Ŀ
ij��ȤС��ͬѧΪ֤��NaOH��Һ��ϡ���ᷢ�����кͷ�Ӧ���Ӳ�ͬ�Ƕ����������ʵ�鷽����������ʵ�飮
����һ������pH��ֽ�ⶨNaOH��Һ��pH���ٵμ����ᣬ����������Һ��ͬʱ�ⶨ�����Һ��pH�������õ�pH��С��С��7����֤��NaOH��Һ��ϡ���ᷢ���˻�ѧ��Ӧ��
��1����pH��ֽ�ⶨ��Һ��pHʱ����ȷ�IJ����ǣ� ��
��2������ǿ������õ�pHС��7�������ɣ� ��
������������NaOH��Һ�еμӼ��η�̪��Һ����Һ�Ժ�ɫ��Ȼ���ٵμ����ᣬ�ɹ۲쵽��ɫ����ʧ����֤��NaOH��Һ��ϡ���ᷢ���˻�ѧ��Ӧ��
����ͬѧ����NaOH��Һ�еμӷ�̪��Һʱ��������һ��������������������Һ�е����̪��Һ����Һ����˺�ɫ������һ�����ɫ����ʧ�ˣ���С����������������ԭ���������²��룺�ٿ����Ƿ�̪��Һ������е�������Ӧ��ʹ��ɫ��ʧ���ڿ���������������Һ������еĶ�����̼��Ӧ��ʹ��ɫ��ʧ��
��1��Ϊ��֤����٣�����ͬѧ��������ʵ�飺�����Ƶ�����������Һ���ȣ�����Һ���Ϸ���һЩֲ���ͣ�Ȼ������ȴ�����Һ�е����̪��Һ��ʵ���С����ȡ��͡�����ֲ���͡�Ŀ���� ��ʵ����������̪��Һ��ɫ��ʧ������е������أ�
��2��Ϊ��֤����ڣ�����ͬѧ��������ʵ�飺ȡ��һ������Na2CO3��Һ�������е����̪��Һ��������ҺҲ���ֺ�ɫ���ɴ˿ɵó�����������ۣ�����1��˵��Na2CO3��Һ�� �ԣ�����2��˵����̪��Һ��ɫ��ʧ������еĶ�����̼�أ�
��3����С��ͬѧͨ���������ϵ�֪��������������ҺŨ�Ⱥܴ�ʱ���ͻ���������������������ʵ��֤���÷�����ȡ�õ�NaOH��ҺŨ�ȹ���ʵ�鷽�� ���ڹ۲쵽������ ��
����������ѧ��Ӧ��ͨ�������������ı仯���ɽ�����Ӧǰ����¶ȱ仯���жϷ�Ӧ�ķ��������NaOH��Һ��ϡ������ǰ���¶��б仯����֤�������˻�ѧ��Ӧ��
����ͬѧ����ͬŨ�ȵ������NaOH��Һ��10mL��ϣ�����
�ȼƲⶨ�����»��ǰ���¶ȵı仯������¼��ÿ�λ��ǰ���¶ȵ�����ֵ��t���������
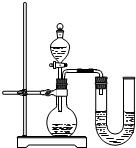
��1������x= ��
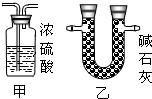
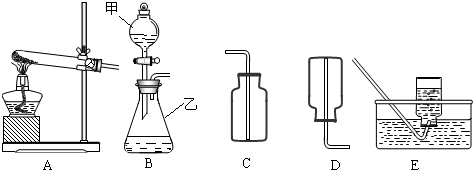
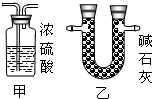
��2��ijͬѧ��ûʹ���¶ȼƵ�����£�ͨ����ͼ��ʾװ�������ʵ�飮���ͬѧ���� �ж�NaOH��Һ��ϡ���ᷢ�����кͷ�Ӧ��
��3������ʵ���е�ϸ�ں������������ʵ���У�ϡ��������ý�ͷ�ι���εμӣ���������Ŀ���� ����ʵ������У�Ҫ�ò��������Ͻ��裬��������Ŀ���� ������ʵ����������ⷢ�������ݳ��֣�����Ϊԭ���� ���ܷ���ʢ��NaOH��Һ���Լ�ƿƿ�ں���Ƥ���ϳ����˰�ɫ��ĩ������������ѧ�Ļ�ѧ֪ʶ�������ְ�ɫ��ĩ�ijɷ��������²��룺�ٿ�����NaOH������Ϊ���ڿ����� �� �ۿ����� ��
��4��Ϊ�˽�һ���о�ʵ���г��ֵ����⣬ȡ��13.3g�������ƹ�����Ʒ��������ˮ�����Һ�������м���200g10%��ϡ���ᣬʹ���ַ�Ӧ�����ɶ�����̼2.2g����
��1����Ʒ���������Ƶ�������
��2�����������Ʒ�Ӧ�������������
��3����ͼ�л������������ʾ������̼�������������ʾ����������Ĺ�ϵͼ��
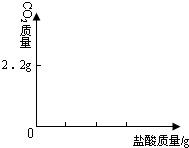
����֪Na2CO3+2HCl�T2NaCl+H2O+CO2����
����һ������pH��ֽ�ⶨNaOH��Һ��pH���ٵμ����ᣬ����������Һ��ͬʱ�ⶨ�����Һ��pH�������õ�pH��С��С��7����֤��NaOH��Һ��ϡ���ᷢ���˻�ѧ��Ӧ��
��1����pH��ֽ�ⶨ��Һ��pHʱ����ȷ�IJ����ǣ�
��2������ǿ������õ�pHС��7�������ɣ�
������������NaOH��Һ�еμӼ��η�̪��Һ����Һ�Ժ�ɫ��Ȼ���ٵμ����ᣬ�ɹ۲쵽��ɫ����ʧ����֤��NaOH��Һ��ϡ���ᷢ���˻�ѧ��Ӧ��
����ͬѧ����NaOH��Һ�еμӷ�̪��Һʱ��������һ��������������������Һ�е����̪��Һ����Һ����˺�ɫ������һ�����ɫ����ʧ�ˣ���С����������������ԭ���������²��룺�ٿ����Ƿ�̪��Һ������е�������Ӧ��ʹ��ɫ��ʧ���ڿ���������������Һ������еĶ�����̼��Ӧ��ʹ��ɫ��ʧ��
��1��Ϊ��֤����٣�����ͬѧ��������ʵ�飺�����Ƶ�����������Һ���ȣ�����Һ���Ϸ���һЩֲ���ͣ�Ȼ������ȴ�����Һ�е����̪��Һ��ʵ���С����ȡ��͡�����ֲ���͡�Ŀ����
��2��Ϊ��֤����ڣ�����ͬѧ��������ʵ�飺ȡ��һ������Na2CO3��Һ�������е����̪��Һ��������ҺҲ���ֺ�ɫ���ɴ˿ɵó�����������ۣ�����1��˵��Na2CO3��Һ��
��3����С��ͬѧͨ���������ϵ�֪��������������ҺŨ�Ⱥܴ�ʱ���ͻ���������������������ʵ��֤���÷�����ȡ�õ�NaOH��ҺŨ�ȹ���ʵ�鷽��
����������ѧ��Ӧ��ͨ�������������ı仯���ɽ�����Ӧǰ����¶ȱ仯���жϷ�Ӧ�ķ��������NaOH��Һ��ϡ������ǰ���¶��б仯����֤�������˻�ѧ��Ӧ��
����ͬѧ����ͬŨ�ȵ������NaOH��Һ��10mL��ϣ�����
�ȼƲⶨ�����»��ǰ���¶ȵı仯������¼��ÿ�λ��ǰ���¶ȵ�����ֵ��t���������
| ��� | ���� | NaOH��Һ | ��t/�� |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |

��1������x=
��2��ijͬѧ��ûʹ���¶ȼƵ�����£�ͨ����ͼ��ʾװ�������ʵ�飮���ͬѧ����
��3������ʵ���е�ϸ�ں������������ʵ���У�ϡ��������ý�ͷ�ι���εμӣ���������Ŀ����
��4��Ϊ�˽�һ���о�ʵ���г��ֵ����⣬ȡ��13.3g�������ƹ�����Ʒ��������ˮ�����Һ�������м���200g10%��ϡ���ᣬʹ���ַ�Ӧ�����ɶ�����̼2.2g����
��1����Ʒ���������Ƶ�������
��2�����������Ʒ�Ӧ�������������
��3����ͼ�л������������ʾ������̼�������������ʾ����������Ĺ�ϵͼ��

����֪Na2CO3+2HCl�T2NaCl+H2O+CO2����