��Ŀ����
����Ŀ�������Ǽ���ʵ������ȡ����ķ���װ�����ռ�װ�ã�

��1��д���������ƣ��� ���� ��
��2��ʵ�����ø��������ȡ�����������ѡȡ�ķ������ռ�װ��Ϊ ������ΪAװ���л�ȱ�� ���÷�Ӧ�Ļ�ѧ����Ϊ ��ʵ����Ҳ����˫��ˮ�����������ȡ��������Ҫ�Ϻõؿ��Ʋ����������ٶȣ�Ӧѡ�÷���װ�� ������ĸ������Ӧ�Ļ�ѧ����ʽΪ �����ж��������ڻ�ѧ��Ӧǰ���Һ������е����������� ������������С�����䡱��
��3��ʵ������п����ϡ������ȡH2�Ļ�ѧ����ʽ ��ʵ������ȡ������̼�Ļ�ѧ����ʽ ��Dװ�����п����ϰ��и�ͻ�����ŵ��� ��
��4������Gװ�ý����ſշ��ռ�����������Ӧ�� ���a����b������ͨ�룮
���𰸡���1������̨������©����
��2��AE��һ������
2KMnO4![]() K2MnO4+MnO2+O2����
K2MnO4+MnO2+O2����
C��2H2O2![]() 2H2O+O2�������
2H2O+O2�������
��3��Zn+H2SO4=ZnSO4+H2����CaCO3+2HCl�TCaCl2+H2O+CO2�������Ʒ�Ӧ�ķ�����ֹͣ��
��4��b��
����������1������̨�dz��õļг�����������©�������Һ��ҩƷ���ʴ�Ϊ������̨������©����
��2������ø����������������Ҫ���ȣ����ȸ������ʱ���Թܿ�Ҫ��һ��������Ϊ�˷�ֹ������ط�ĩ���뵼�ܣ��������ܶȱȿ������ܶȴ�������ˮ��������������ſ���������ˮ���ռ��������ſ������ռ�������Ƚϸ�������˫��ˮ�Ͷ��������������Ͳ���Ҫ���ȣ����ж��������ڻ�ѧ��Ӧǰ���Һ������е��������������Һ©�����Կ��Ʒ�Ӧ���ٶȣ��ʴ�Ϊ��AE��һ������2KMnO4![]() K2MnO4+MnO2+O2����C�� 2H2O2
K2MnO4+MnO2+O2����C�� 2H2O2![]() 2H2O+O2�������
2H2O+O2�������
��3��ʵ��������п����ϡ�����ڳ����·�Ӧ�������ģ�����������ˮ���ܶȱȿ������ܶ�С����˿�������ˮ���������ſ������ռ���ʵ������ȡCO2�����ڳ����£��ô���ʯ��ʯ��ʯ��ϡ������ȡ�ģ�̼��ƺ����ụ�ཻ���ɷ������Ȼ��ƺ�ˮ�Ͷ�����̼����˲���Ҫ���ȣ�Dװ�����п����ϰ��и�ͻ�����ŵ��ǣ����Ʒ�Ӧ�ķ�����ֹͣ���ʴ�Ϊ��Zn+H2SO4=ZnSO4+H2����CaCO3+2HCl�TCaCl2+H2O+CO2�������Ʒ�Ӧ�ķ�����ֹͣ��
��4������Gװ�ý����ſշ��ռ�����������Ӧ�ӳ��ܽ��룬��Ϊ�������ܶȱȿ����ʴ�Ϊ��b��

 �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�����Ŀ����ʵ��̽�����ϣ���ʦ����ͬѧ��һ����ɫ��δ���÷�ĩ��ͭ�ۺ����������е�һ�ֻ����֣�ͬѧ��Ϊ��ȷ���÷�ĩ�ijɷ֣���������̽�����������̽�����ش����⣮
��������롿����l����ɫ��ĩ��ͭ�ۣ� ����2����ɫ��ĩ���������ۣ�
����3����ɫ��ĩ�� ��
��ʵ��̽����ijͬѧΪ��һ��ȷ����ɫ��ĩ����ɣ���ȡ�÷�ĩ5.0gװ��Ӳ�ʲ������У�����ͼװ����ͨ����н���ʵ�飮��ʼʱ����ͨ��CO���壬��һ��ʱ����ټ���ʹ���ַ�Ӧ������Ӧ��ȫ��ֹͣ���ȣ��Լ���ͨCO����ֱ����������ȴ����Ӧǰ��������װ�ú����ʵ������������������±���
��Ӧǰ | ��Ӧ�� | |
�� �� | �����ܺͺ�ɫ��ĩ��������Ϊ37.3g | �����ܺ������ʵ�������Ϊ36.1g |
�� �� | ϴ��ƿ����ʢ��Һ ��������Ϊ180.0g | ϴ��ƿ��ƿ������ ��������Ϊ183.1g |
���������ۡ�
��1��Ӧ��ѡ�� ���ʵ������������ȷ����ɣ���ѡ����һ��������� �����ռ������������ú�ɫ��ĩ������Ǽ��� ������ţ�������
��2��д��Aװ���з�����Ӧ�Ļ�ѧ����ʽ ��ʵ���й۲쵽Aװ���е�����Ϊ ��
��3��Ϊ�˷�ֹ��Һ��������ʵ��ֹͣ����ǰ�Ƿ���Ҫ�ȶϿ�A��B�����Ӵ������жϲ�˵�����ɣ� ��
����˼���ۡ�
��1���ӻ����Ƕȣ���װ�������ز���֮��������ΪӦ����θĽ��� ��
��2��ʵ�鿪ʼʱҪ��ͨ��CO����װ���еĿ����ž����ټ��ȣ��Է�������ը������װ���еĿ������ž��ķ����� ��

����Ŀ��ij����С����ѧϰ���鱾�����������������IJⶨ��ʵ�飬֪��P2O5��������ŷ��ڿ����У������Կ��������Ⱦ�����ԶԸ�ʵ������˸Ľ���
��ͼ��ʾ����������ע������ɵ��ܱ�ϵͳ�ڹ���25mL������Ȼ���װ�к��IJ����ܼ��ȣ�ͬʱ�����ƶ�����ע�����Ļ��������������ڵĺ��ױ�ɰ��̣��ҽϳ�ʱ������һ���仯��ֹͣ���ȣ�����ȴ�����£�������ȫ������һ��ע�����ڣ��ش��������⣺
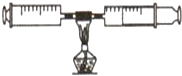
��1����ʵ��ļ��ȹ����У����滺���ƶ�����ע������Ŀ�� ��
��2��д������ȼ�յĻ�ѧ��Ӧ����ʽ ��
��3��С����ʵ�������£�
��Ӧǰע��������������� | ��Ӧ��ע��������������� |
25mL | 22mL |
�ɴ����ݿ�����������ⶨ�Ŀ������������������ 2l%�����������=����������
��ɸ�ʵ���������ԭ������� ������ţ���
A��û�н��滺���ƶ�����ע����������
B������ʱû����ȴ�����£�
C�����������̫�٣�
D��װ��©��
��4��ͨ�������ʵ�飬��ѧ���IJ����������ij�ɷֺ����ķ����� ��



