题目内容
【题目】某同学设计如下几组实验,探究某些酸、碱、盐之间的复分解反应能否发生。
已知:BaSO4是白色固体,难溶于水,也不与盐酸反应。
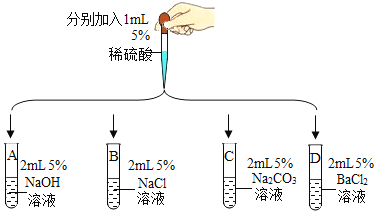
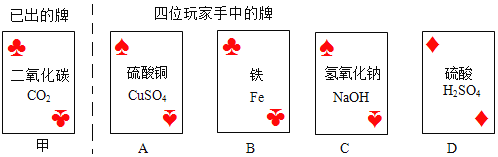
(第一组)选取5种溶液,如图所示进行实验。
实验 |
| ||
现象及结论 | 试管A和B中无明显现象,不能确定反应是否发生 | 试管C中产生_____(填实验现象)。复分解反应已发生 | 试管D中有白色沉淀产生。复分解反应已发生 |
解释 | 试管C中减少的微粒是_____(填微粒符号) | 反应的化学方程式为_____ | |
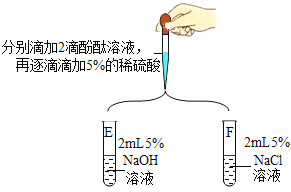
(第二组)对试管A和B中是否发生反应再探究,如图所示进行实验。
实验 |
| |
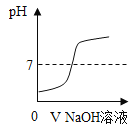
现象及结论 | 试管E中,滴加酚酞溶液后,溶液由无色变为红色;滴加一定量稀硫酸后,溶液由红色变为无色。复分解反应已发生 | 试管F中始终无明显现象,不能确定反应是否发生 |
解释 |
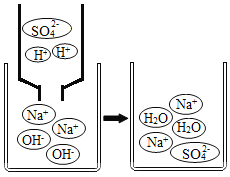
从微观粒子变化的角度分析试管E中反应的实质是_____ | |
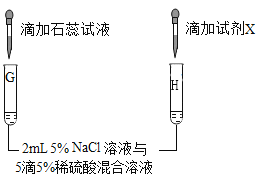
(第三组)对试管B中是否发生反应继续探究,如图所示进行实验。
实验 |
| |
现象及结论 | 试管G中溶液变红 | 向试管H中滴加_____(填“试剂X”的化学式)溶液后,有白色沉淀产生 |
解释 | 该实验的目的是为了检验试管G的溶液中存在 | 溶液中有SO42-存在 |
结论 | NaCl溶液与稀硫酸不发生复分解反应 | |
【答案】气泡 CO32- H2SO4+BaCl2=BaSO4↓+2HCl 氢氧根离子与氢离子结合生成了水分子 BaCl2(或Ba(NO3)2、Ba(OH)2) H+
【解析】
(1)由于稀硫酸与碳酸钠反应生成了硫酸钠、二氧化碳和水,所以3号试管中的实验现象是:有气泡产生;
(2)试管C中反应实质碳酸根离子与氢离子反应生成二氧化碳和水,所以试管C中减少的是碳酸根离子,符号为CO32-;
(3)试管D中发生复分解反应是稀硫酸与氯化钡反应生成了硫酸钡沉淀和盐酸,反应的化学方程式为:H2SO4+BaCl2═BaSO4↓+2HCl;
(4)从微观粒子变化的角度分析,该反应的实质是:氢氧根离子与氢离子结合生成了水分子;
(5)由于稀硫酸电离出的氢离子能使石蕊试液变成红色,所以该实验的目的是为了检验试管G的溶液中存在H+;
(6)钡离子与硫酸根离子会产生白色的硫酸钡沉淀,故向H试管中滴加BaCl2(或Ba(NO3)2、Ba(OH)2)溶液检验溶液中是否有SO42-存在。

 教学练新同步练习系列答案
教学练新同步练习系列答案