题目内容
【题目】为保护绿水青山,将工业残留的钡渣(主要成分为BaCO3)进行无害化处理,制取化工原料硫酸钡,主要的流程如下:
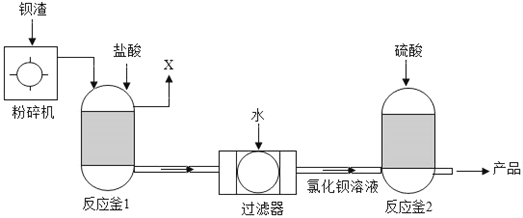
请回答下列问题:
(1)粉碎钡渣的目的是_____。
(2)反应釜1的气体X是_____。
(3)反应釜2中发生反应的化学方程式为_____。
(4)碳酸钡也可以通过复分解反应直接转化为硫酸钡,其反应方程式为_____。
【答案】增大反应物的触面积,加快反应的进行 二氧化碳(CO2) BaCl2+H2SO4═BaSO4↓+2HCl BaCO3+H2SO4═BaSO4↓+CO2↑+H2O
【解析】
化学反应的速率和反应物的状态和反应条件有关,碳酸钡和稀盐酸反应生成氯化钡和水和二氧化碳,氯化钡与稀硫酸反应生成硫酸钡沉淀和盐酸。
(1)粉碎钡渣的目的是增大反应物的触面积,加快反应的进行。
(2)反应釜1发生的反应是碳酸钡和稀盐酸反应生成氯化钡和水和二氧化碳,气体X是二氧化碳。
(3)反应釜2中发生反应的是氯化钡与稀硫酸,反应生成硫酸钡沉淀和氯化氢,化学方程式为BaCl2+H2SO4═BaSO4↓+2HCl。
(4)碳酸钡也可以通过复分解反应直接转化为硫酸钡,其反应方程式为BaCO3+H2SO4═BaSO4↓+CO2↑+H2O。

 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案【题目】通过下列实验操作和现象能得出相应结论的是( )
实验操作 | 现象 | 结论 | |
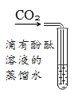
A | 向收集满CO2的软塑料瓶中,加入约 | 塑料瓶变瘪 | CO2能与NaCl反应 |
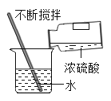
B | 50℃时,将19gKCl固体加入50g蒸馏水中,完全溶解后缓慢降温 | 降温至20℃时开始有晶体析出 | 20℃时,KCl的溶解度为38g |
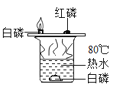
C | 将白磷浸没在热水中,再向热水中的白磷通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧需要的条件之一 |
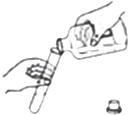
D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是CH4 |
A. AB. BC. CD. D