题目内容
(3分)为测定某瓶久置的氢氧化钠固体中碳酸钠的含量,取该久置的氢氧化钠固体10 g,加入90.5 g水完全溶解后,再缓慢加入30 g石灰乳(氢氧化钙和水的混合物),测得生成沉淀的质量与加入石灰乳的质量关系如右图所示。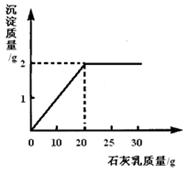
试计算:
(1)该氢氧化钠固体中碳酸钠的质量分数。
(2)恰好完全反应时,所得溶液中溶质的质量分数。
(1)21.2% (2)8%
解析试题分析:根据图象可知,加入20g石灰乳与碳酸钠恰好完全反应,生成碳酸钙沉淀2g,然后利用碳酸钙的质量代入化学反应方程式计算碳酸钠的质量;恰好完全反应后溶液的溶质为氢氧化钠,其质量为反应生成的加上原来的,溶液质量利用质量守恒得到,最后计算溶质的质量分数。
解:设久置的氢氧化钠中碳酸钠质量为x,反应生成氢氧化钠的质量为y
Na2CO3 + Ca(OH)2 ="==" CaCO3↓+ 2NaOH
106 100 80
x 2 g y 解得x =" 2.12" g
解得x =" 2.12" g  解得y =" 1.6" g
解得y =" 1.6" g
(1)该氢氧化钠固体中碳酸钠的质量分数= =21.2%
=21.2%
(2)恰好完全反应时,所得溶液中溶质的质量分数= =8%
=8%
答:氢氧化钠固体中碳酸钠的质量分数为21.2%,恰好完全反应时,所得溶液的溶质质量分数为8%。
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
点评:此题是关于化学方程式及溶质质量分数的计算题,主要是利用图表及反应方程式来分析和解决化学计算中的有关问题,要求学生有较强的识图能力和数据分析能力,解题的关键是找出相关的化学反应,并依据已知量对未知的应求量进行求解计算,解题要规范。

练习册系列答案
相关题目