题目内容
【题目】海水是巨大的资源宝库,化学元素种类高达80多种。从中提取镁的简易流程如图:

请结合你所学知识回答下列问题:
(1)操作a的名称_____。
(2)试剂A为石灰乳,它所含阴离子的符号为_____。
(3)试剂B与Mg(OH)2反应制取MgCl2的化学反应方程式为_____,该反应的基本反应类型是_____
(4)利用海水制食盐,一般采用_____(填“蒸发结晶”或“降温结晶”)的方法。
【答案】过滤 OH﹣ Mg(OH)2+2HCl=MgCl2+2H2O 复分解反应 蒸发结晶
【解析】
(1)操作a是分离液体与难溶性固体的方法,即过滤;
(2)石灰乳的主要成分是氢氧化钙,是由钙离子与氢氧根离子构成的化合物,其中的阴离子是氢氧根离子,其符号为:OH﹣;
(3)根据图示可知试剂B与氢氧化镁反应生成氯化镁,所以B是盐酸,还会生成水,反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O;该反应是由两种化合物相互交换成分生成两种新的化合物,属于复分解反应;
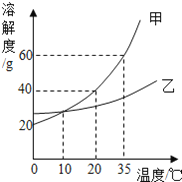
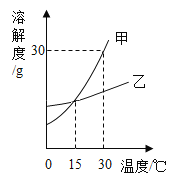
(4)因为氯化钠的溶解度受温度的影响不大,所以利用海水制食盐,一般采用蒸发结晶的方法。

【题目】“84”消毒液在日常生活中使用广泛,具有漂白、杀菌、消毒功效。某化学兴趣小组对一瓶敞口久置的“84”消毒液成分产生兴趣,在老师的指导下进行如下探究:
(提出问题)该敞口久置的“84”消毒液中溶质有哪些?
(查阅资料)“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO为有效成分,有腐蚀性并易与空气中CO2反应(2NaClO+CO2+H2O=2HClO+Na2CO3)。次氯酸(HClO)溶液和次氯酸钠(NaClO)溶液都具有漂泊、杀菌、消毒功效。HClO不稳定,受热或光照易分解。
(分析讨论)小组同学经过讨论,认为:一定含有____,可能还有NaClO、HClO、Na2CO3中的一种或几种。
(设计方案)为验证猜想,设计如下方案:
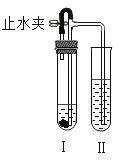
实验操作 | 实验现象 | 结论 |
Ⅰ、向盛有有色布条的烧杯中滴加该消毒液适量,放置一段时间 | 布条不褪色 | 该消毒液中___ |
Ⅱ、另取该消毒液少量于试管中,滴加足量氯化钙溶液,震荡 | _ | 该消毒液中含有Na2CO3 |
实验Ⅱ中的反应化学方程式为____;
(得出结论)综上所述,该敞口久置的“84”消毒液中溶质有__。
(交流反思)生活中,“84”消毒液贮藏时应注意_。一般不要“84”消毒液对蔬菜、水果进行消毒,其原因可能是_。
(拓展延伸)(1)次氯酸钠与稀硫酸可发生复分解反应,化学方程式为____
(2)次氯酸钠与盐酸反应可生成有毒的氯气,日常生活中“84”消毒液不能与洁厕灵(主要成分为盐酸)混合使用。