题目内容
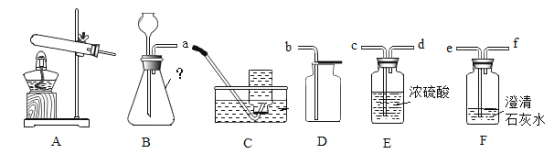
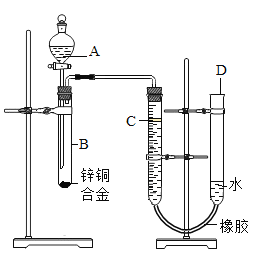
【题目】下列为实验室制取气体的发生和收集装置。
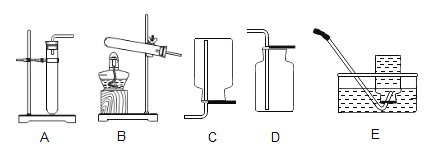
(1)实验室用高锰酸钾制取氧气的化学方程式是_____,发生装置选择_____(填字母序号)。
(2)氧气可选用D装置进行收集,其原因是_____。
【答案】2KMnO4![]() K2MnO4+MnO2+O2↑ B 氧气的密度比空气大
K2MnO4+MnO2+O2↑ B 氧气的密度比空气大
【解析】
(1)根据反应物、生成物和反应条件书写化学方程式;根据反应物的状态、反应发生需要的条件及特殊要求选择发生装置;
(2)根据氧气的性质进行分析。
(1)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑; 该反应属于固、固加热型,适合用装置B作发生装置;
K2MnO4+MnO2+O2↑; 该反应属于固、固加热型,适合用装置B作发生装置;
(2)氧气可选用D装置进行收集,其原因是氧气的密度比空气大。
故答案为:
(1)2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(2)氧气的密度比空气大。

 名校课堂系列答案
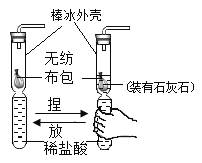
名校课堂系列答案【题目】暖宝宝是一种常见的防寒用品,如图是其包装上的使用说明。小英见后思考:暖宝宝中的主要成分有哪些?发热的原因是什么?

(1)探究一:暖宝宝的主要成分是什么?
小英打开未使用过的暖宝宝,倒出其中的粉末,发现呈黑色。
[提出猜想]该黑色粉末可能含有炭粉、铁粉、氧化铜、四氧化三铁中的一种或几种。
[初步验证]将磁铁靠近黑色粉末,部分被吸引。
[查阅资料]I.四氧化三铁具有磁性,能被磁铁吸引。
II.氧化铜和稀硫酸反应产生蓝色溶液。
由资料I可知,该黑色粉末可能含有___________________________________________。
[进行实验]
实验编号 | 实验操作 | 实验现象 |
① | 取适量黑色粉末加入足量稀硫酸 | 部分固体溶解,有气泡产生,溶液无蓝色 |
② | 取实验①的残渣灼烧,并将内壁涂有澄清石灰水的小烧杯罩在其上方 | 澄清石灰水变浑浊 |
[得出结论]由实验①可知,该黑色粉末肯定含有_____________________,肯定不含有_____________________。由实验②可知,该黑色粉末肯定含有_____________________。
(2)探究二:暖宝宝的发热原理是什么?
[提出猜想]可能发生了铁生锈的反应。
[进行实验小英打开一包使用过的暖宝宝,看到里面有块状红褐色物质,取少量红褐色物质洗净、烘干后碾成粉末,与足量的木炭粉末充分混合后装到试管中,给混合物加强热至完全反应,观察到_____________________,待试管冷却后向其中加入稀盐酸,观察到_____________________。
进一步证实了她的猜想。
[反思应用]根据铁生锈的条件,保存暖宝宝的时候应该注意:_____________________。