题目内容
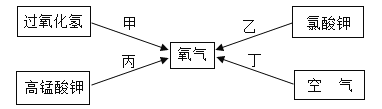
【题目】下图中的甲、乙、丙表示初中化学常见的物质,已知甲是一种酸,图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物已略去。
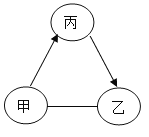
(1)甲溶液中一定含有的离子是______(写化学符号)。
(2)若丙是常温下最常见的液体,乙是可用来改良酸性土壤的碱,则甲与乙反应的基本类型是____________反应;“丙 → 乙”的化学方程式为____________。
(3)若甲为硫酸,乙、丙都含铜元素,则乙可能是______(填化学式);写出符合“甲- 丙”的一个反应的化学方程式___________________。
【答案】H+ 复分解反应 CaO +H2O = Ca(OH)2 Cu(OH)2或CuCO3 H2SO4 + CuO= CuSO4 + H2O (或H2SO4 + Cu(OH)2= CuSO4 + 2H2O)
【解析】
根据甲、乙、丙表示初中化学常见的物质,则:
(1)因为甲是一种酸,甲溶液中一定含有的离子是H+;
(2)若丙是常温下最常见的液体,则为水;乙是可用来改良酸性土壤的碱,则为氢氧化钙,则甲与乙反应,可能为稀盐酸与氢氧化钙反应,故反应的基本类型是复分解反应;“丙→乙”的化学方程式为CaO+H2O═Ca(OH)2。
(3)若甲为硫酸,乙、丙都含铜元素,则乙可能是Cu(OH)2;符合“甲→丙”的一个反应的化学方程式为:H2SO4+CuO=CuSO4+H2O。
故答案为:
(1)H+.(2)复分解反应;CaO+H2O═Ca(OH)2。
(3)Cu(OH)2;H2SO4+CuO=CuSO4+H2O。

练习册系列答案
相关题目