题目内容
【题目】如图是甲乙两物质的溶解度曲线,下列说法正确的是( ) 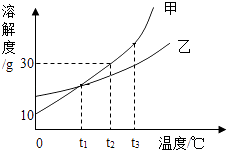
A.甲的溶解度大于乙
B.t1℃时,甲乙饱和溶液中溶质质量相等
C.t2℃时,将10g甲加入50g水中,得到60g饱和溶液
D.将t3℃时的甲乙饱和溶液降温到t1℃,甲乙溶液中溶质质量分数相等
【答案】D
【解析】解:A、当大于t1℃时,甲的溶解度大于乙,不指明温度不正确,故选项错误; B、t1℃时,甲乙饱和溶液中溶质质量相等,应该是t1℃时,相等质量的甲乙饱和溶液中溶质质量相等,故选项错误;
C、t2℃时,将10g甲加入50g水中,得到60g不饱和溶液,不是饱和溶液,故选项错误;
D、将t3℃时的甲乙饱和溶液降温到t1℃,甲乙的溶解度相等,因此甲乙溶液中溶质质量分数相等,故选项正确;
故选D
【考点精析】通过灵活运用固体溶解度曲线及其作用和溶质的质量分数、溶解性和溶解度的关系,掌握1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和);溶质质量分数 =溶质质量/溶液质量*100% ;溶解度=溶质质量/溶剂质量*100g (必须选取饱和溶液);溶液质量=溶质质量(克)+溶剂质量(克) ;对于饱和溶液,溶液质量分数w = S/(S+100);所以溶解度S = 100/(1/w-1)即可以解答此题.

 阅读快车系列答案
阅读快车系列答案【题目】小明同学在家中带来了一个废弃的水龙头,其成分为黄铜(铜锌合金),为了测定黄铜中铜的质量分数,在老师的指导下做了如下实验,有关实验数据记录如表:
实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
所取黄铜样品的质量(g) | 32.0 | 32.0 | 32.0 | 32.0 |
加入稀硫酸的质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
反应后烧杯内剩余物质的质量(g) | 71.9 | a | 151.7 | 191.7 |
请分析实验数据,完成下列计算
(1)第2次实验中a的数值为 .
(2)该黄铜样品中铜的质量分数?(请写出计算过程,计算结果精确到0.1%)
(3)第4此实验中,充分反应后溶液中溶质的成分为(写化学式).
【题目】根据问题填空:
(1)实验室制得的二氧化碳中常含有水蒸气和少量酸雾,为了获得纯净的二氧化碳可选用如图中的套装置来净化. 
其中左瓶中应盛;右瓶中应盛 .
(2)向氢氧化钠溶液中通入适量二氧化碳后,仅使溶液中 50%的氢氧化钠反应,反应后溶液中 CO ![]() 和 OH的个数比为 .
和 OH的个数比为 .
(3)现将石灰石样品 15g 与 105.4g 稀盐酸放入烧杯中充分反应(杂质不溶于水也不与稀 盐酸反应),反应时间与反应前后烧杯内物质的质量变化如表所示:
反应时间/s | 20 | 40 | 60 | 80 | 100 | 120 |
质量/g | 119.52 | 118.64 | 117.76 | 116.88 | 116 | 116 |
请计算回答:①样品中碳酸钙的质量分数.(计算结果保留 1 位小数)
②反应后所得溶液中溶质的质量分数.


