题目内容
【题目】下列说法正确的有( )
①氦的原子示意图为![]() ,镁的原子示意图为
,镁的原子示意图为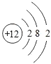 ,由于它们的最外层电子数相同,所以化学性质相似
,由于它们的最外层电子数相同,所以化学性质相似
②已知A+3B=2C+3D中,已知2.3克A跟4.8克B恰好反应生成4.4克C。又已知D的相对分子质量为18,则A的相对分子质量为46
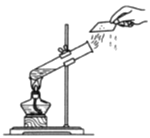
③实验室现需要250毫升的集气瓶收集一瓶100毫升的氧气,小明设计了如图装置进行收集;

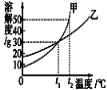
④足量红磷在密闭容器中燃烧,反应变化关系图像是:

A.1个
B.2个
C.3个
D.4个
【答案】B
【解析】
①氦原子核外只有一个电子层,最外层电子数为2, 是稳定结构,不易得失电子;镁的原子最外层电子数小于4个,易失去电子,它们最外层电子数相同,但化学性质不相似,错误;
②生成D的质量=2.3g+4.8g-4.4g=2.7g。设A的相对分子质量为M。
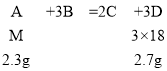
![]()
M=46g,正确;
③氧气不易溶于水,密度比水小,从储气的角度应该是把水压出,所以是短进长出,正确;
④足量红磷在密闭容器中燃烧,容器内的温度升高压强增大,冷却后容器内的压强小于原来容器内的压强错误。故选B。

【题目】以下是教材中关于水的一些实验,根据所学水的知识回答下列问题:
|
|
|
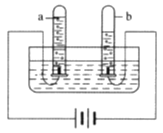
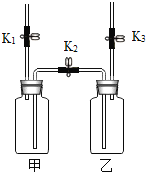
A.水的沸腾 | B.水的电解 | C.水的净化 |
(1)对于实验A中水的沸腾,下列说法正确的是_____(填字母)。
A 水分子之间间隔不变 B 水分子的运动速率加快
C 水分子保持不变 D 保持水化学性质的粒子是氢原子和氧原子
(2)实验B水的电解中试管b得到的气体是_____(填名称)。
(3)实验C中净化水时,小卵石和石英砂的作用是_____。
(4)水是一种重要的化工原料。氯碱工业通过电解饱和氯化钠溶液的方法制取烧碱(NaOH),其中发生的主要反应是氯化钠和水在通电的条件下生成氢氧化钠、氢气、氯气(Cl2),该反应的化学方程式为_____。