��Ŀ����
����Ŀ���������Ƽ��������ԭ���ǣ��Ƚ�����ͨ�뱥��ʳ��ˮ�У��ٽ�ѹ���Ķ�����̼ͨ�뱥�͵İ���ˮ���õ�̼�����ƾ��壬����õ���̼�����ƾ��������ȷֽ���Ƶô�� 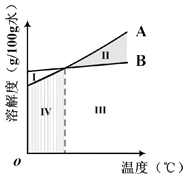
NaCl��NH4Cl���ܽ�ȱ���
�¶ȣ��棩 | 0 | 10 | 20 | 30 | 40 | 50 | |
�ܽ�� | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | |
������ṩ����Ϣ���ش����⣺
��10��ʱ��NaCl���ܽ������
��ͼ�У���ʾNH4Cl���ܽ�����������A����B����
�۳���20��ʱ�����Ƶı���ʳ��ˮ����������Ϊ �� ��ʳ��ˮ���¶���ߣ���Һ�����ʵ���������Ҳ����ߣ���ʵ�������������ڳ����½��У�����������������
����NaCl��NH4Cl��Һ��������������ͬ����ʾ�䱥��״̬�ĵ���ͼ�п���λ�ڵ���������ѡ�� I��II��III��IV����
��������ͨ�백����������̼����Ҫ�����Щ������ܽ�ȣ������������е�����ѡ���ţ�
A������ѹǿ B�������¶� C������ˮ����
���𰸡�35.8g��A��26.5%���¶�����ʳ�ε��ܽ�����߲��࣬�����������Ҳ��߲��࣬�����ܴ�III��IV��A
���������⣺��10��ʱ��NaCl���ܽ����35.8g�� ���35.8g������ͼ���ܽ�����������ʵ��ܽ�ȿ�֪����ʾNH4Cl���ܽ��������A��
���A���۳���20��ʱ�����Ƶı���ʳ��ˮ����������Ϊ�� ![]() ��100%=26.5%��
��100%=26.5%��
��ʳ��ˮ���¶���ߣ���Һ�����ʵ���������Ҳ����ߣ���ʵ�������������ڳ����½��У����������������¶�����ʳ�ε��ܽ�����߲��࣬�����������Ҳ��߲��࣬�����ܴ�
���26.5%���¶�����ʳ�ε��ܽ�����߲��࣬�����������Ҳ��߲��࣬�����ܴ���NaCl��NH4Cl��Һ��������������ͬ����ʾ�䱥��״̬�ĵ���ͼ�п���λ�ڵ�������III��IV��������ΪIII��IV���Ȼ��ƺ��Ȼ�淋��ܽ���п�����ȣ���I��III���������ʵ��ܽ�Ȳ�������ȣ�
���III��IV����������ͨ�백����������̼����Ҫ�����Щ������ܽ�ȣ������������е�������ѹǿ���������¶��ܹ�������Щ�������ܽ�ȣ�����ˮ�����ܸı���Щ������ܽ�ȣ�
���A��
�����㾫�������ù����ܽ�����������ú������ܽ�ȵ�Ӱ�����ض���Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪1������ָ���¶�ʱ���ʵ��ܽ�ȣ��������ܽ���ж��ܽ��ԣ�2���Ƚ���ͬ�¶�ʱ����һ���¶ȷ�Χ�ڣ���ͬ�����ܽ�ȵĴ�С��3���ȽϺ�ȷ�����ʵ��ܽ�����¶�Ӱ��ij̶ȣ����ݴ�ȷ�����ʽᾧ����������ᴿ�ķ�����4��ȷ����Һ��״̬�������벻���ͣ���������ܽ��:��1�������ܽ�ȵĶ��壺��ѹǿΪ101kPa��һ���¶�ʱ�������ܽ���1���ˮ��ﵽ����״̬ʱ�������������2��Ӱ�����أ� ����������ʢ��¶ȣ��¶�Խ�ߣ������ܽ��ԽС����ѹǿ��ѹǿԽ�������ܽ��Խ����