题目内容
实验室需用氯酸钾制取氧气,化学方程式: 2 KClO3 KCl + 3O2↑。现将 29.4g 氯酸钾与 5.6g 二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.4g。回答:
KCl + 3O2↑。现将 29.4g 氯酸钾与 5.6g 二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.4g。回答:
(1)生成氧气的质量是多少?
(2)剩余固体中氯化钾质量是多少?
(3)固体剩余物中是否还含有氯酸钾?
 KCl + 3O2↑。现将 29.4g 氯酸钾与 5.6g 二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.4g。回答:
KCl + 3O2↑。现将 29.4g 氯酸钾与 5.6g 二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.4g。回答:(1)生成氧气的质量是多少?
(2)剩余固体中氯化钾质量是多少?
(3)固体剩余物中是否还含有氯酸钾?
(1) 9.6 g;(2)14.9g;(3)含有
试题分析:根据质量守恒定律反应后质量减少的质量就是生成的氧气的质量,以氧气的质量为突破口计算其它量即可
解:(1)生成氧气的质量="29.4" g +5.6 g - 25.4 g =" 9.6" g
(2)设剩余固体中氯化钾的质量为m
2KClO3
 2KCl + 3O2↑
2KCl + 3O2↑2×74.5 3×32
m 9.6 g
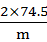 =
=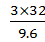
m ="14.9" g
(3)∵14.9 g+5.6 g="20.5" g<25.4 g
∴剩余固体中还含氯酸钾

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
 2CuSO4 + 2H2O)现有溶质的质量分数为10%的稀硫酸(其中含溶质98 g)与铜恰好完全反应,假设硫酸不和其他杂质反应,求反应后硫酸铜溶液中溶质的质量分数。(最后结果精确到0.1%)
2CuSO4 + 2H2O)现有溶质的质量分数为10%的稀硫酸(其中含溶质98 g)与铜恰好完全反应,假设硫酸不和其他杂质反应,求反应后硫酸铜溶液中溶质的质量分数。(最后结果精确到0.1%)
