题目内容
硝酸铵是常用的氮肥,化学式为NH4NO3,求:
(1)NH4NO3的相对分子质量为
(2)NH4NO3中氮、氢、氧元素质量比为
(3)NH4NO3中氮元素的质量分数为多少?
(4)200g NH4NO3含有氮元素质量为多少?
(1)NH4NO3的相对分子质量为
(2)NH4NO3中氮、氢、氧元素质量比为
(3)NH4NO3中氮元素的质量分数为多少?
(4)200g NH4NO3含有氮元素质量为多少?
考点:相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=
×100%,进行分析解答.
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:(1)硝酸铵的相对分子质量为14×2+1×4+16×3=80.
(2)硝酸铵中氮元素、氢元素、氧元素的质量比为(14×2):(1×4):(16×3)=7:1:12.
(3)硝酸铵中氮元素的质量分数为
×100%=35%.
(4)200g NH4NO3含有氮元素质量为200g×35%=70g.
故答案为:(1)80;(2)7:1:12;(3)35%;(4)70g.
(2)硝酸铵中氮元素、氢元素、氧元素的质量比为(14×2):(1×4):(16×3)=7:1:12.
(3)硝酸铵中氮元素的质量分数为
| 14×2 |
| 80 |
(4)200g NH4NO3含有氮元素质量为200g×35%=70g.
故答案为:(1)80;(2)7:1:12;(3)35%;(4)70g.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
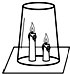 上海“1115特大火灾”造成了严重的人员伤亡,这一悲剧为高层住宅的消防安全敲响了警钟.艾桦雪同学为了研究火灾逃生策略,进行了如图所示模拟实验.将两支燃着的蜡烛罩上茶杯,一会儿后高的蜡烛先熄灭,低的蜡烛后熄灭,同时还观察到茶杯内壁变黑.由此我们可以得到启发:从着火燃烧的高层房间中逃离,下列方法中正确的是( )
上海“1115特大火灾”造成了严重的人员伤亡,这一悲剧为高层住宅的消防安全敲响了警钟.艾桦雪同学为了研究火灾逃生策略,进行了如图所示模拟实验.将两支燃着的蜡烛罩上茶杯,一会儿后高的蜡烛先熄灭,低的蜡烛后熄灭,同时还观察到茶杯内壁变黑.由此我们可以得到启发:从着火燃烧的高层房间中逃离,下列方法中正确的是( )| A、用湿毛巾捂住鼻子站在原地等待救援 |
| B、成站立姿势跑出 |
| C、湿毛巾捂住鼻子沿墙角伏低身子迅速爬向门外 |
| D、打开窗户跳出 |
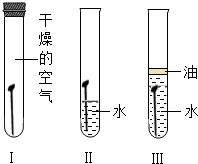 为探究铁生锈的影响因素,某兴趣小组做了如图实验.
为探究铁生锈的影响因素,某兴趣小组做了如图实验.
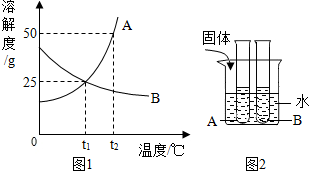 图1是A、B、两种固体物质的溶解度曲线,图2是将装有A、B两种物质饱和溶液的试管放入盛有t1℃水的烧杯中,根据图象和有关信息判断,回答以下问题.
图1是A、B、两种固体物质的溶解度曲线,图2是将装有A、B两种物质饱和溶液的试管放入盛有t1℃水的烧杯中,根据图象和有关信息判断,回答以下问题.
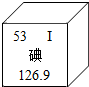 人体内约有50多种元素,其中碘元素是人体必需的微量元素.(1)碘元素的原子序数是
人体内约有50多种元素,其中碘元素是人体必需的微量元素.(1)碘元素的原子序数是