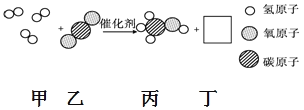
题目内容
【题目】下列说法错误的是( )
A. 5g硫和5g氧完全反应后,生成物质量为10g
B. 2.3g某物质在空气中完全燃烧,生成4.4g二氧化碳和2.7g水,则该物质一定只含有碳、氢两种元素
C. 等质量的二氧化硫和三氧化硫中,硫元素的质量比为5:4
D. 足量的镁和锌分别与质量相等、质量分数相等的稀盐酸充分反应,生成氢气的质量相等
【答案】B
【解析】
A、根据硫和氧气反应的化学方程式可以知道:硫和氧气在反应中的质量比为1:1,所以5g硫和5g氧气完全反应后,生成物质量为10g,选项正确;
B、先根据反应前后元素的种类不变,确定:该物质中一定含有碳、氢两种元素,可能含有氧元素。再根据反应前后元素的质量相等,来确定是否含有氧元素。
二氧化碳中碳的质量为:4.4g×![]() ×100%=1.2g;
×100%=1.2g;
水中氢的质量为:2.7g×![]() ×100%=0.3g;
×100%=0.3g;
碳元素与氢元素质量之和为1.2g+0.3g=1.5g;
由于1.5g<2.3g,所以该物质中一定含有氧元素,且含有氧的质量为2.3g﹣1.5g=0.8g。
故可判断该化合物中一定含有C、H、O元素,选项错误;
C、设二氧化硫和三氧化硫的质量为1,则有相同质量的二氧化硫和三氧化硫中硫元素的质量比为: ![]() 选项正确;
选项正确;
D、足量的镁和锌分别与质量相等、质量分数相等的稀盐酸充分反应,盐酸被消耗,产生氢气的质量由酸决定,故参与反应的HCl的质量相等,产生的氢气的质量就相等。选项正确。
故选:B。

【题目】火锅是我国独创的美食,历史悠久。火锅常用的一种燃料是固体酒精。某化学兴趣小组的同学对“固体酒精”产生了好奇,对其成分进行探究。请你回答下列问题。
(查阅资料)
a.固体酒精也被称为"酒精块"或固体燃料块。固体酒精并不是固体状态的酒精而是将酒精、硬脂酸和氢氧化钠按一定的质量比混合制成。
b.酒精的化学式为C2H5OH;
c.氯化钡、氯化钠溶液均呈中性。
d. BaCl2+Na2CO3=BaCO3↓+2NaCl 生成的BaCO3为白色固体
(提出问题)
(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是不是显碱性?
(2)固体酒精中的氢氧化钠是否变质及变质的程度如何?
(实验探究1)酒精的水溶液是不是显碱性
同学们取少量酒精溶液于试管中,滴加紫色石蕊溶液,未观察到紫色石蕊变为蓝色,说明酒精溶液_______(填“显”或“不显”)碱性。
(实验探究2)固体酒精中的氢氧化钠是否变质及变质的程度如何
①固体酒精中的氢氧化钠是否变质,同学们先取少量固体酒精于烧杯中,加入足量水溶解后滴加足量的稀盐酸,观察到__________现象,说明氢氧化钠已变质.请写出氢氧化钠在空气中变质的化学方程式______________。
②为进一步确定氢氧化钠的变质程度,分组进行探究。
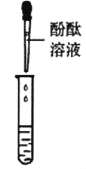
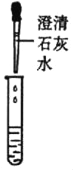
甲组同学取烧杯上层清液于两支试管中,按如图所示进行实验。
实验方案 |
|
|
实验现象 | 溶液变红 | 产生__ |
实验结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
乙组同学认为甲组实验不能证明清液中一定有氢氧化钠,理由是__。他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后,静置,取上层清液,滴加酚酞溶液,酚酞溶液变红。
(反思交流)乙组实验中加足量氯化钡溶液的目的是________。
(实验结论]小组同学经过讨论,一致认为该固体酒精中的氢氧化钠部分变质。
【题目】氯气(Cl2)是黄绿色气体,氯气溶于水部分以Cl2分子存在于溶液中,部分与水反应Cl2+H2O=HCl+HClO.产物中,次氯酸HClO是一种弱酸.氯气溶于水所得溶液称为氯水.把品红试纸(染有品红颜料的滤纸)放入氯水中,品红试纸褪色.如图是实验室制取氯气的成套装置图,请填空:

(1)仪器X的名称是:_____.
(2)从反应物的状态和反应条件看,装置甲属于_____型气体发生装置.
(3)氯气在装置丁中被收集,其收集方法为_____,装置戊中可得到氯水.
(4)晓红对“氯水使品红试纸褪色”产生兴趣,她所在的学习小组进行了如下探究,请你一起来完成:
(提出问题)氯水中的什么成分使品红试纸褪色?
(猜 想)猜想1:氯水中的水使品红试纸褪色;
猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色;猜想4:氯水中的_____(填化学式)使品红试纸褪色.
(实验探究)
实 验 操 作 | 实 验 现 象 | 结 论 |
①把品红试纸放入水中 | _____ | 猜想1不成立 |
②把品红试纸放入干燥的氯气中 | 试纸不褪色 | 猜想2不成立 |
③_____ | 试纸不褪色 | 猜想3不成立 |
(结 论)学习小组通过讨论,找到了氯水中使品红试纸褪色的物质.
(反 思)向氯水中滴加几滴紫色石蕊试液,会观察到的现象是_____.
【题目】松花蛋,又称皮蛋、变蛋。其中一种加工工艺的主要原料配方为:鸭蛋10Kg,水10Kg,生石灰1.2Kg,纯碱0.53Kg,食盐0.35Kg.加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再放入鸭蛋浸渍。
请回答下列问题:
(1)生石灰加入沸水中,水能持续保持沸腾,其原因是_____。
(2)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为_____色。
(3)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动。
(提出问题)料液中含有哪些溶质?
(交流讨论)①一定含有NaOH、NaCl
②可能还含有其它溶质;
甲同学推断只有Ca(OH)2
乙同学推断只有Na2CO3
丙同学推断有Ca(OH)2、也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是_____(用化学方程式表示)。
(实验探究)
实验步骤 | 实验现象 |
取少量上层料液,滴加过量_____ | 无明显现象 |
另取少量上层料液,滴加_____溶液 | 产生白色沉淀 |
(探究结论)_____同学的推断是正确的。