题目内容
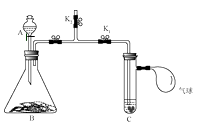
【题目】鸡蛋壳的主要成分是碳酸钙(其他成分不与水也不与盐酸反应)。为了测定鸡蛋壳碳酸钙的含量,进行如下实验:
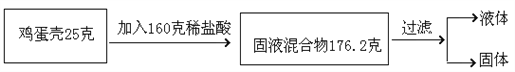
(1)生成二氧化碳的质量是__________。
(2)计算鸡蛋壳中碳酸钙的质量分数为_________。
【答案】 8.8g 80%
【解析】(1)根据质量守恒定律计算生成二氧化碳的质量;(2)根据碳酸钙的质量和鸡蛋壳的质量计算碳酸钙的质量分数。(1)生成二氧化碳的质量为:25g+160g﹣176.2g=8.8g;
(2)设CaCO3的质量为x。
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x8.8g
![]()
x=20g
故鸡蛋壳中碳酸钙的质量分数=![]() ×100%=80%
×100%=80%
答:(1)生成二氧化碳的质量是8.8g;(2)计算鸡蛋壳中碳酸钙的质量分数为80%。

练习册系列答案
相关题目