题目内容
【题目】下表是元素周期表中二、三周期的元素,请回答有关问题.

(1)下列各组具有相似化学性质的元素是___(填字母序号)
A.Na、Cl B.O、S C.F、Ne D.C、Si
(2)写出一条第三周期元素原子的核外电子排布规律:______.
(3)第 17 号元素与第 13 号元素的原子形成化合物的化学式为_______.
(4)某粒子的结构示意图为 ,当 x-y=8 时,该粒子的符号为______.
,当 x-y=8 时,该粒子的符号为______.
【答案】BD 最外层电子数从左向右依次递增(合理即可) AlCl3 S2-
【解析】
(1)元素原子的最外层电子数决定元素的化学性质,故具有相似化学性质的元素原子的最外层电子数相同,故本题选BD;
(2)由元素周期表可知,第三周期元素原子的核外电子排布规律最外层电子数从左向右依次递增;
(3)由元素周期表可知,第17号元素是氯元素,第13号元素是铝元素,故两种元素形成的化合物为氯化铝,氯元素形成化合物时为-1价,铝元素形成化合物时为+3价,故第 17 号元素与第 13 号元素的原子形成化合物的化学式为AlCl3;
(4)某粒子的结构示意图为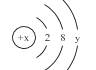 ,当 x-y=8 时,x=8+y,故该粒子核外电子数比质子数多2,该粒子有三个电子层,故该粒子为硫离子,符号为S2-。
,当 x-y=8 时,x=8+y,故该粒子核外电子数比质子数多2,该粒子有三个电子层,故该粒子为硫离子,符号为S2-。

【题目】某化学兴趣小组对氧气的制取进行了进一步探究。
(1)用高锰酸钾制氧气,对比用向上排空气法和排水法收集到的氧气的纯度。
(进行实验)
①用向上排空气法收集氧气:将带火星的木条放在集气瓶口,当_________时证明氧气集满,用传感器测定集气瓶中氧气的体积分数。重复该实验3次并记录数据。
②用排水法收集氧气:氧气能用排水法收集的原因是____,用传感器测定集气瓶中氧气的体积分数。重复该实验3次并记录数据。
氧气的收集方法 | 向上排空气法 | 排水法 | ||||
氧气的体积分数/% | 79.7 | 79.6 | 79.9 | 90.0 | 89.8 | 89.3 |
氧气的平均体积分数/% | 79.7 | 89.7 | ||||
(实验分析)不考虑操作失误的因素,用排水法也收集不到纯净的氧气,其主要原因是__________。
(2)用过氧化氢溶液制氧气,探究不同催化剂催化过氧化氢分解的效果。
(查阅资料)
①MnO2、Cr2O3、Fe2O3、CuO、S对过氧化氢的分解均具有催化作用。
②海藻酸钠可以作为催化剂的载体支架,形成负载不同催化剂的海藻酸钠微球。
(进行实验)
①制备五种负载不同催化剂(MnO2、Cr2O3、Fe2O3、CuO、S)的海藻酸钠微球,每个微球大小相同,且负载催化剂的质量相等。
②取30粒负载某种催化剂的海藻酸钠微球与20mL质量分数为5%的过氧化氢溶液,在锥形瓶中迅速混合发生反应,实验装置如图1,采集200s内压强数据,绘制曲线如图2。

(实验分析)
①每次实验时,海藻酸钠微球数应相同的原因是_________。
②本实验中,通过一段时间内______来反映生成氧气的快慢。
③本实验中,负载MnO2的微球显示了良好的催化效果,60s时竟将橡皮塞弹飞,在图2中对应的曲线是_______(填“a”或“b”);负载_______的微球催化效果较好,反应温和;负载Fe2O3、Cr2O3的微球催化效果一般;负载_______的微球催化能力最弱。