题目内容
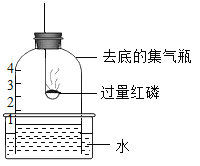
【题目】某课外活动小组的同学在实验室做锌和浓硫酸反应的实验。(其反应方程式![]() )甲同学认为产生的气体中只有SO2,乙同学认为除SO2外,还可能有H2.为了验证甲、乙两同学的判断,他们设计了如图所示的装置(设锌与浓硫酸共热时产生的气体为X气体发生装置已略去)
)甲同学认为产生的气体中只有SO2,乙同学认为除SO2外,还可能有H2.为了验证甲、乙两同学的判断,他们设计了如图所示的装置(设锌与浓硫酸共热时产生的气体为X气体发生装置已略去)
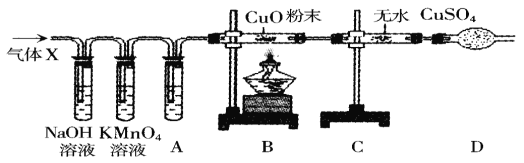
已知二氧化硫可以与高锰酸钾溶液反应,溶液会褪色。
(1)NaOH溶液的作用是(用化学方程式表示)_____。高锰酸钾溶液的作用是_____。
(2)乙同学认为还可能产生氢气的理由是_____。
(3)A中盛装的溶液是_____,其作用是_____。
(4)可以证明气体X中含有H2的实验现象是:_____。
【答案】2NaOH+SO2=Na2SO3+H2O 证明二氧化硫被氢氧化钠溶液完全吸收 锌和浓硫酸反应产生SO2和H2O,硫酸浓度变稀,一段时间后成为稀硫酸,与锌反应生成H2 浓硫酸 吸收水分 B中黑色粉末变红,C中硫酸铜粉末变蓝
【解析】
(1)氢氧化钠能够与二氧化硫反应生成亚硫酸钠和水,此处氢氧化钠溶液的作用是吸收二氧化硫,故反应的化学方程式写为:2NaOH+SO2=Na2SO3+H2O;
二氧化硫可以与高锰酸钾溶液反应,溶液会褪色,前面的氢氧化钠溶液用来吸收二氧化硫,所以高锰酸钾溶液用来证明二氧化硫被氢氧化钠溶液完全吸收,故填证明二氧化硫被氢氧化钠溶液完全吸收。
(2)锌和浓硫酸反应产生SO2和H2O,硫酸浓度变稀,一段时间后成为稀硫酸,稀硫酸与锌反应生成H2,故填锌和浓硫酸反应产生SO2和H2O,硫酸浓度变稀,一段时间后成为稀硫酸,与锌反应生成H2。
(3)为避免气体中的水对实验产生干扰,需要对反应前的气体进行干燥,装置A中盛放干燥剂,由图可知,该干燥剂是浓硫酸,故填浓硫酸;
浓硫酸具有吸水性,能够吸收气体中的水分,使气体变干燥,故填吸收水分。
(4)气体中含有氢气,则氢气与氧化铜在高温的条件下反应生成铜和水,观察到的现象是B中粉末由黑变红,反应后的气体通过装置C时,水与无水硫酸铜反应生成硫酸铜晶体,观察到的现象是C中硫酸铜粉末变蓝,故填B中黑色粉末变红,C中硫酸铜粉末变蓝。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某同学想在实验室里用NaOH溶液制取Na2CO3溶液。
查阅资料:①CO2通入NaOH溶液时极易因CO2过量而产生NaHCO3,且无明显现象
②NaHCO3溶液煮沸时不会发生分解
③![]()
④Ca(HCO3)2可溶于水
制取步骤:①量取两份50mL相同浓度的NaOH溶液备用;
②用一份50mLNaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
③小心煮沸②溶液1~2分钟;
④_____,即得Na2CO3溶液。
实验探究:为了检验制得的溶液是否为纯净的Na2CO3溶液,请你与该同学一起完成下列实验探究:
实验步骤 | 实验现象 | 实验结论 | |
取少量制得的溶液于试管中,加入过量的_____溶液 | 产生白色沉淀 | 原来溶液含有Na2CO3 | |
将上步实验所得混合物进行过滤,将滤液分成两份 | 取其中一份加入足量的_____ | 无气泡产生 | 原来制得的溶液中不含_____ |
取另一份加入MgCl2溶液 | _____ | 原来制得的溶液中不含NaOH | |
结论:所制得的溶液为纯净的Na2CO3溶液
评价与反思:有人认为实验步骤③④的顺序对调,即先混合,再煮沸,更合理。你认为对吗?_____请说明理由:_____。