题目内容
【题目】某化学小组Ⅰ探究用大理石和稀盐酸反应制取二氧化碳气体,并进行性质实验.如图是有关实验的部分装置,请根据要求回答问题:
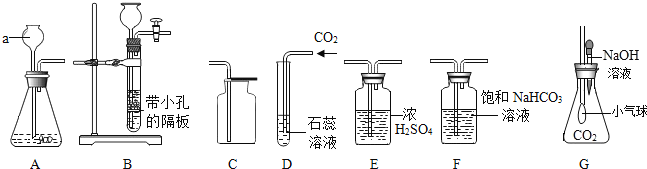
(1)a仪器的名称为_____;甲同学用A和C组合制取二氧化碳,乙同学用B和C组合制取二氧化碳,你认为哪个组合更便于控制反应_____(填写甲或乙);该装置还能用来制取某种常见气体,其反应原理是_____;该气体的验满方法是_____.
(2)甲同学利用装置D进行性质实验时,观察到紫色石蕊试液变红色,将红色液体充分加热未能重新变为紫色,你认为可能的原因是_____;为使上述红色液体加热后能重新变为紫色,在气体通入装置D之前可接入上图装置_____(填字母序号);在该装置中发生的主要化学反应方程式为_____;
(3)乙同学将CO2通入到氢氧化钠溶液中,无明显现象,经过思考讨论后,设计了如图G装置,使该反应有了明显现象,则该装置G中的现象为_____.
【答案】长颈漏斗 乙 2H2O2![]() 2H2O+O2↑ 将带火星的木条放在集气瓶口,木条复燃,证明集满 盐酸具有挥发性,挥发出的氯化氢使紫色石蕊变红色 F NaHCO3+HCl=NaCl+H2O+CO2↑ 气球变鼓
2H2O+O2↑ 将带火星的木条放在集气瓶口,木条复燃,证明集满 盐酸具有挥发性,挥发出的氯化氢使紫色石蕊变红色 F NaHCO3+HCl=NaCl+H2O+CO2↑ 气球变鼓
【解析】
(1)根据实验室常用仪器的名称和题中所指仪器的作用,B装置可以通过装置内压强的改变实现固体和液体的分离,该装置制取气体的反应是固体和液体,反应条件是常温,可以用过氧化氢制取氧气,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,氧气有助燃性进行分析;
(2)根据碳酸分解生成水和二氧化碳,氯化氢溶于水生成盐酸,碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳进行分析;
(3)根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析.
(1)通过分析题中所指仪器的作用可知,a是长颈漏斗,B装置可以通过装置内压强的改变实现固体和液体的分离,所以乙组合更便于控制反应,该装置制取气体的反应是固体和液体,反应条件是常温,可以用过氧化氢制取氧气,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2![]() 2H2O+O2↑,氧气有助燃性,所以该气体的验满方法是:将带火星的木条放在集气瓶口,木条复燃,证明集满;
2H2O+O2↑,氧气有助燃性,所以该气体的验满方法是:将带火星的木条放在集气瓶口,木条复燃,证明集满;
(2)碳酸分解生成水和二氧化碳,氯化氢溶于水生成盐酸,所以将红色液体充分加热未能重新变为紫色,可能的原因是:盐酸具有挥发性,挥发出的氯化氢使紫色石蕊变红色,碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,所以在气体通入装置D之前可接入上图装置F,化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑;
(3)氢氧化钠和二氧化碳反应生成碳酸钠和水,装置内气压减小,所以该装置G中的现象为气球变鼓.

 每日10分钟口算心算速算天天练系列答案
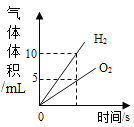
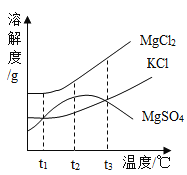
每日10分钟口算心算速算天天练系列答案【题目】下列4个图象中,不能正确反映对应变化关系的是( )
|
|
|
|
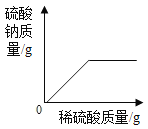
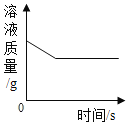
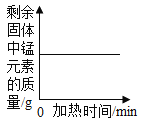
A、向一定质量的氢 氧化钠溶液中加 入稀硫酸至过量 | B、向一定质量的稀 硫酸中加入锌片 | C、加热一定质量的 高锰酸钾固体 | D、将水通电电解一段时间 |
A.AB.BC.CD.D
【题目】有一包白色固体,可能含有氯化钠、氢氧化钠、碳酸钠、硫酸钠和硝酸钡中的一种或几种,为探究其组成,某合作学习小组设计方案并进行了如下实验:
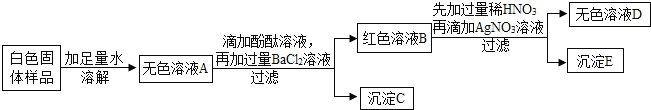
(1)小晶同学通过上述实验推知:白色固体样品中一定不含有____________(用化学式表示,下同)。
(2)为确定白色固体样品中可能存在的物质,小燕对沉淀C进行实验。
实验操作 | 现象 | 结论 |
取少量沉淀C于试管中,加入过量稀硝酸。 | ___________。 | 白色固体样品中一定含有碳酸钠和硫酸钠。 |
(3)上述实验中红色溶液B的溶质,除酚酞外,还一定含有______________________,用化学方程式表示红色溶液B变成无色溶液D的原因:_____________________________。
(4)小虎同学认为白色固体中还有物质不能确认其是否存在,经过小组讨论后得出一致意见:如要确认,只需将上述实验方案中所加的一种试剂换为另一种试剂即可,你认为修改方案为_______________。