题目内容
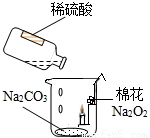
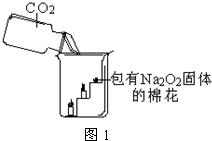
过氧化钠(Na2O2)是一种淡黄色固体,常温下与二氧化碳发生反应的化学方程式为2Na2O2+2CO2═2Na2CO3+O2.现将沾有Na2O2固体的棉花放入如图的烧杯中,再缓慢向烧杯中倒入适量稀硫酸,使之与杯底的Na2CO3反应产生CO2气体,发现蜡烛火焰熄灭,沾有Na2O2固体的棉花燃烧起来.下列从实验获得的信息中,你认为不正确的是( )
A.棉花具有可燃性
B.CO2不支持蜡烛燃烧,但能支持棉花燃烧
C.Na2CO3与CO2反应放热,使温度达到棉花的着火点
D.棉花燃烧证明“可燃物、氧气、温度达到着火点”是燃烧必须同时具备的条件
【答案】分析:根据题意可知,稀硫酸与杯底的Na2CO3反应产生CO2气体,并释放出热量;因二氧化碳不支持燃烧,所以蜡烛熄灭;又因棉花上的Na2O2与生成的二氧化碳反应释放出热量,使棉花达到着火点,所以棉花燃烧起来.我们可以据此分析选项的正确与否.
解答:解:A、沾有Na2O3固体的棉花燃烧起来,就说明棉花具有可燃性,故正确;
B、蜡烛火焰熄灭,是因为稀硫酸与杯底的Na2CO3反应产生CO2气体,二氧化碳不支持燃烧,所以蜡烛熄灭;而二氧化碳不支持燃烧是它的特性,并不因燃烧物的不同而改变.所以CO2不支持蜡烛燃烧,同样不支持棉花燃烧,故错误;
C、沾有Na2O2固体的棉花之所以燃烧起来,就是因为Na2O2与生成的二氧化碳反应释放出热量,使棉花达到着火点,所以棉花燃烧起来.故正确;
D、棉花能够燃烧就是因为棉花是可燃物,并与氧气(或空气)接触,稀硫酸与杯底的Na2CO3反应释放的热量,使棉花达到了着火点.所以我们由此可知“可燃物、氧气、温度达到着火点”是燃烧必须同时具备的条件,故正确.
故选B.
点评:本题以实验探究的形式考查燃烧的条件,在考查同学们化学知识的同时,又要同学们从所给的资料中提取信息,这就要同学们具备语文学科的基本知识能力.
解答:解:A、沾有Na2O3固体的棉花燃烧起来,就说明棉花具有可燃性,故正确;
B、蜡烛火焰熄灭,是因为稀硫酸与杯底的Na2CO3反应产生CO2气体,二氧化碳不支持燃烧,所以蜡烛熄灭;而二氧化碳不支持燃烧是它的特性,并不因燃烧物的不同而改变.所以CO2不支持蜡烛燃烧,同样不支持棉花燃烧,故错误;
C、沾有Na2O2固体的棉花之所以燃烧起来,就是因为Na2O2与生成的二氧化碳反应释放出热量,使棉花达到着火点,所以棉花燃烧起来.故正确;
D、棉花能够燃烧就是因为棉花是可燃物,并与氧气(或空气)接触,稀硫酸与杯底的Na2CO3反应释放的热量,使棉花达到了着火点.所以我们由此可知“可燃物、氧气、温度达到着火点”是燃烧必须同时具备的条件,故正确.
故选B.
点评:本题以实验探究的形式考查燃烧的条件,在考查同学们化学知识的同时,又要同学们从所给的资料中提取信息,这就要同学们具备语文学科的基本知识能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


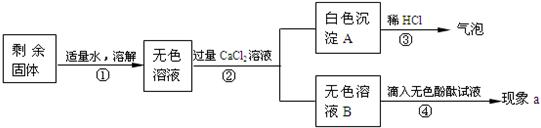
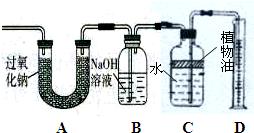 23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.
23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.