题目内容
【题目】如图为池州正在建设海绵城市的一个场景,图2是建设工程中使用的透水砖. 
(1)图2中的透水砖可对雨水起到作用,实验室进行该操作时,使用到的玻璃仪器有:玻璃棒、烧杯、 .
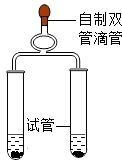
(2)在盛有品红溶液的锥形瓶中加入几块烘烤过的木炭,振荡,会观察到锥形瓶內品红溶液 , 那么将木炭放入硬水中,充分振荡,硬水会变成软水吗? . 家庭中可采用什么方法降低水的硬度 .
(3)利用下列指定的仪器和药品,应用控制变量法设计对比实验比较活性炭和木炭的吸附性强弱:
试管、棉花、活性炭、木炭、玻璃棒、品红溶液(仪器和药品的数量不限制)
实验操作方法 | 观察到的现象 | 实验结论 |
实验表明活性炭的吸附性比木炭的吸附性强 |
(注意:实验操作方法用图片或用文字描述都可以,观察到的现象一定要能支持实验结论)
【答案】
(1)过滤;漏斗
(2)红色逐渐消失;不会;煮沸
(3)分别取10mL品红溶液放入试管,各加入5g活性炭和5g木炭,搅拌、静置5min;加入5g活性炭的试管滤液比加入5g木炭的试管滤液颜色浅
【解析】解:(1)透水砖可对雨水起到过滤作用,实验室进行该操作时,使用到的玻璃仪器有:玻璃棒、烧杯、漏斗.(2)木炭具有疏松多孔结构,具有吸附性,能吸附色素,将几块烘烤过的木炭投入到滴有少量红墨水的水中,振荡后可观察到红色逐渐消失.硬水和软水的区别在于所含的钙镁离子的多少,那么将木炭放入硬水中,充分振荡,硬水不会变成软水;常用煮沸或蒸馏的方法来降低水的硬度,生活着常用煮沸的方法使硬水软化.(3)分别取10mL品红溶液放入试管,各加入5g活性炭和5g木炭,搅拌、静置5min,加入5g活性炭的试管滤液比加入5g木炭的试管滤液颜色浅,说明活性炭的吸附性比木炭的吸附性强.
答案:(1)过滤;漏斗;(2)红色逐渐消失;不会;煮沸;(3)
实验操作方法 | 观察到的现象 | 实验结论 |
分别取10mL品红溶液放入试管,各加入5g活性炭和5g木炭,搅拌、静置5min | 加入5g活性炭的试管滤液比加入5g木炭的试管滤液颜色浅 | 实验表明活性炭的吸附性比木炭的吸附性强 |
【考点精析】解答此题的关键在于理解水的净化的相关知识,掌握水的净化效果由低到高的是静置、吸附、过滤、蒸馏(均为物理方法),其中净化效果最好的操作是蒸馏;既有过滤作用又有吸附作用的净水剂是活性炭,以及对硬水与软水的理解,了解硬水和软水的鉴别方法:用肥皂水,有浮渣产生或泡沫较少的是硬水,泡沫较多的是软水.

【题目】某校化学研究性学习小组探究气体制取的实验原理与方法.
(1)甲同学将课本的基础知识进行整理如图,请你帮助他完成相关内容. 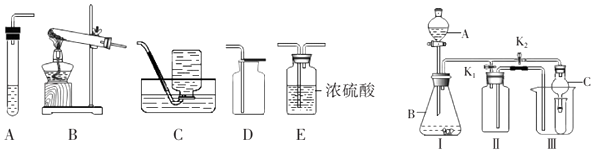
制取气体 | 所需要品 | 装置连接顺序 | 反应化学方程式 |
干燥的二氧化碳 | 大理石和稀盐酸 |
|
|
(2)乙同学设计的实验装置(如图),既可用于制取气体,又可用于验证物质性质.当打开 K1、关闭 K2 时, 利用 I、Ⅱ装置可直接进行的实验是(填序号).
①大理石与稀盐酸反应制取二氧化碳
②锌与稀硫酸反应制取氢气
(3)丙同学认为在不改变 I、Ⅱ、Ⅲ装置的仪器及位置的前提下,该装置可用于过氧化钠(Na2O2)固体与水 反应制取氧气,另一产物为氢氧化钠,则该反应的化学方程式为;她的改进措施是 .
(4)丁同学打开 K2、关闭 K1 , 利用 I、Ⅲ装置来验证生成的二氧化碳中含有水蒸气,此时 C 中盛放的物质是 , 可以观察到的现象是 .
(5)对用氯酸钾和二氧化锰的混合物制取 O2后的固体残渣(假定已完全反应)作如下回收处理: ①通过以下四步实验操作回收二氧化锰.正确操作的先后顺序是(填写选项序号a. 烘干b. 溶解c.过滤d.洗涤
②用所得氯化钾晶体配制 50g 质量分数为 5%的氯化钾溶液,需要氯化钾的质量为 g
③过滤、蒸发时都需用到的仪器是(填序号).
A. 酒精灯B. 烧杯C. 玻璃棒D.漏斗E.量筒
(6)小明用 6.5g 可能含有铜、铝、铁、镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成 0.2g 氢气,则此锌粉中一定含有的金属杂质是 .
【题目】在过氧化氢溶液的分解反应中,二氧化锰能作催化剂.
(1)下列有关催化剂的说法正确的是(填序号).
A.在化学反应后其质量减小
B.在化学反应后其化学性质发生了变化
C.能增大生成物的质量
D.能改变化学反应速率
(2)某化学兴趣小组的同学知道二氧化锰能做过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质是否也可作过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白.
【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,是否有其他物质也能作催化剂?
【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作催化剂.
【实验探究】
实验操作 | 实验现象 | 实验结论 | |
实验一 | 有少量气泡 | 常温下过氧化氢溶液分解速率很慢. | |
实验二 | 在装有过氧化氢溶液的试管中加入少量氧化铜,然后将带火星的木条伸入试管中 | 在过氧化氢的分解反应中氧化铜改变分解速率 |
(3)【得出结论】氧化铜能作过氧化氢分解的催化剂. 【反思提高】经过讨论,有的同学认为只有上述实验,不能证明氧化铜能作过氧化氢分解的催化剂,还要补充一个探究实验三:
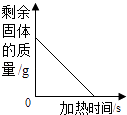
【实验三目的】探究氧化铜在反应前后质量是否改变.
【实验步骤】①准确称量氧化铜(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、、称量,在过滤实验中使用的玻璃棒一起有烧杯、玻璃棒、;④对比反应前后氧化铜的质量.
(4)【交流讨论】如果在反应前后氧化铜质量 , 则说明氧化铜可以作过氧化氢分解的催化剂.
(5)【提出新的问题】但还有同学认为,要证明氧化铜能作过氧化氢分解的催化剂,上述三个实验还不准确够,还需要再增加一个探究实验四: 【实验四目的】探究 .
(6)【拓展探究】同学们对二氧化锰和氧化铜对过氧化氢溶液分解的催化作用能力做了更深入的探究,设计如下四组实验进行比较,其中观察效果最差的是(选填序号)
|
|
|
|
第一组 | 第二组 | 第三组 | 第四组 |
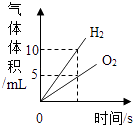
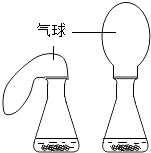
A.第一组同时实验,观察比较反应过程中两个气球体积的变化
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
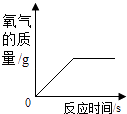
C.第三组分两次实验,看木条是否能复燃
D.第四组分两次实验,比较收集一定体积的气体所需要的时间.