题目内容
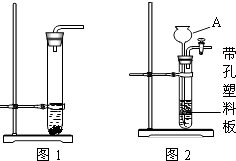
【题目】某研究性学习小组利用如图所示实验装置进行了以下探究实验.步骤如下: 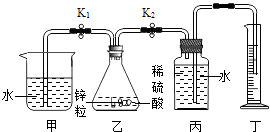
①检查装置气密性,加入锌粒和稀硫酸;
②关闭K2、打开K1 , 待气泡连续均匀产生,立即关闭K1、打开K2 , 并开始计时;
③待丁中收集到10mL水,结束计时;
④换不同溶质质量分数、不同体积的稀硫酸,与质量相同的同一种锌粒重复上述实验;
⑤将每次实验的数据记录于下表:
硫酸用量(mL) | 40 | 40 | 20 | 20 | 20 | 10 | 10 |
硫酸的溶质质量分数(%) | 9.8 | 39.2 | 9.8 | 19.6 | 39.2 | 19.6 | 39.2 |
收集所用时间 | 4′03 | 1′36 | 4′12 | 3′30 | 1′40 | 3′42 | 1′48 |
(1)写出乙中反应的化学方程式:;
(2)该实验的目的是:;
(3)上述实验证明:对该反应中氢气产生的速率有显著影响;
(4)若要快速制取大量氢气,可在乙中加入几滴硫酸铜溶液,但加入的量不可过多,原因是:(用化学方程式表示).
【答案】
(1)Zn+H2SO4═ZnSO4+H2↑
(2)探究溶液的溶质质量分数对反应速率的影响
(3)硫酸的溶质质量分数
(4)Zn+CuSO4═ZnSO4+Cu
【解析】解:(1)锌与稀硫酸反应生成的是硫酸锌和氢气,故填:Zn+H2SO4═ZnSO4+H2↑;(2)换用不同的溶质质量分数的稀硫酸与相同的锌粒反应产生相同体积的氢气,该实验想探究的是溶质质量分数对反应速率的影响,故填:探究溶液的溶质质量分数对反应速率的影响;(3)在金属活动性顺序中,锌排在铜的前面,能与硫酸铜反应生成硫酸锌和铜,故填:Zn+CuSO4═ZnSO4+Cu.
【考点精析】关于本题考查的氢气的制取和检验和书写化学方程式、文字表达式、电离方程式,需要了解氢气的实验室制法原理:Zn + H2SO4 = ZnSO4 +H2↑;Zn + 2HCl = ZnCl2 +H2↑不可用浓盐酸的原因 浓盐酸有强挥发性 ;不可用浓硫酸或硝酸的原因 浓硫酸和硝酸有强氧化性;注意:a、配平 b、条件 c、箭号才能得出正确答案.