题目内容
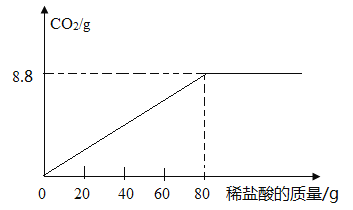
【题目】我州地处武陵山区,具有丰富的天然石灰石、大理石(主要成分是碳酸钙)资源,纯度高、硬度大,是优质的建筑材料.为测定某地天然大理石中碳酸钙的含量(杂质不与稀盐酸反应),某化学兴趣小组成员取25g样品,加入一定溶质质量分数的稀盐酸,测得的实验数据如图所示。
(1)求样品中碳酸钙的质量分数;
(2)所加稀盐酸的溶质质量分数.
【答案】(1)80% (2)18.25%
【解析】
试题分析:根据图示,可知反应生成的气体二氧化碳的质量为8.8g,然后根据化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑中CO2与CaCO3、HCl的质量关系,分别求出CaCO3、HCl的质量,进一步计算样品中碳酸钙的质量分数以及所加稀盐酸的溶质质量分数
解:设碳酸钙的质量为x,HCl的质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 8.8g
(1)100:44=x:8.8g x=20g
样品中碳酸钙的质量分数=20g/25g×100%=80%
(2)73:44=y:8.8g y=14.6g
所加稀盐酸的溶质质量分数=14.6g/80g×100%=18.25%

练习册系列答案
相关题目