��Ŀ����
����Ŀ����ͼ�����л�ѧ�У�����ѧϰ����ͼ���кͷ�Ӧ��ʵ����H++OH��=H2O��������ʵ�ʲμӷ�Ӧ�����ӷ�������ʾ��Ӧ��ʽ�ӽ����ӷ���ʽ�����ӷ���ʽ����дһ�㰴���²��裺����Na2SO4��BaCl2��ӦΪ����
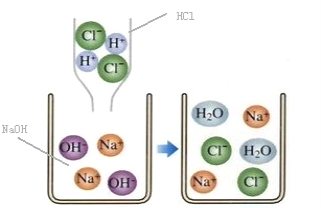
��д����Ӧ�Ļ�ѧ����ʽ��Na2SO4+BaCl2=BaSO4��+2NaCl
�ڰ�������ˮ����������д��������ʽ�������ܵ����ʡ������ˮ�����û�ѧʽ��ʾ����������ʽ�ɸ�д�ɣ�2Na++SO42��+Ba2++2Cl��=BaSO4��+2Na++2Cl��
��ɾȥ����ʽ���߲��μӷ�Ӧ�����ӣ�Ba2++SO42-=BaSO4��
�ܼ�鷽��ʽ���߸�Ԫ�ص�ԭ�Ӹ����͵�������Ƿ���ȣ�
��ش�
��1�����и����е����ӣ�������Һ�д����������
A��K+ H+ SO42�� OH�� B��Na+ Ca2+ CO32�� NO3��
C��Na+ H+ Cl�� CO32�� D��Na+ Cu2+ Cl�� SO42��
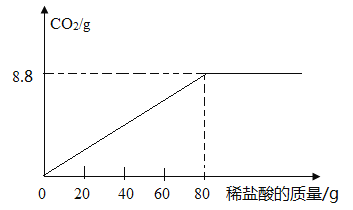
��2��д��ϡ�������ʯ��ʯ����������Ӧ�����ӷ���ʽ ��
��3��д��һ�������ӷ���ʽMg+2H+=Mg2++H2�����Ӧ�Ļ�ѧ����ʽ ��
��4���ᡢ�����ˮ��Һ�з����ĸ��ֽⷴӦʵ���Ͼ������ֻ���������Һ����������ӵķ�Ӧ��ֻҪ�߱��������������������� ���ɣ���Ӧ���ܷ�����
���𰸡���1��D ��2��CaCO3+2H+=Ca2++H2O+CO2��
��3��Mg+H2SO4=MgSO4+H2����Mg+2HCl=MgCl2+H2�� ��4��ˮ
��������
�����������1����ν���ӹ��棬�������Ӽ����ϲ����γɳ����������ˮ�������ֽⷴӦ��������A��H+��OH-�����γ�H2O�����ܹ��棬B��CO32-��Ca2+�����γ�CaCO3���������ܹ��棬C��H+��CO32-�����γ�H2CO3�����ȶ����ֽ����������̼��ˮ�����ܹ��棬��ѡ D
��2�������������Ϣ�ڰ�������ˮ����������д��������ʽ�������ܵ����ʡ������ˮ�����û�ѧʽ��ʾ��ϡ�������ʯ��ʯ����������Ӧ�����ӷ���ʽ��CaCO3+2H+=Ca2++H2O+CO2��
��3��һ�������ӷ���ʽMg+2H+=Mg2++H2�����Ӧ�Ļ�ѧ����ʽ��Mg+H2SO4=MgSO4+H2����Mg+2HCl=MgCl2+H2��
��4���ᡢ�����ˮ��Һ�з����ĸ��ֽⷴӦʵ���Ͼ������ֻ���������Һ����������ӵķ�Ӧ��ֻҪ�߱���������������������ˮ���ɣ���Ӧ���ܷ���