题目内容
在我校实验室实施的扬州市2011年中考化学实验操作考查刚刚落下帷幕.实验考查中H2O2分解制氧气为何不采用MnO2作催化剂?同学们为之展开了探究.
I、他们首先配制实验所需的50mL、6%的H2O2溶液.
[配制溶液]
现有一瓶新购置的双氧水,标签如图所示.
(1)若用这瓶双氧水来配置6%的医用双氧水1500g,需要这种双氧水的质量是多少克?
(2)另有一瓶5个月前购进的相同规格的双氧水,经检测,已缓慢分解放出了9.6g氧气,求现在剩余的该瓶溶液中溶质的质量分数.
II、然后同学们又比较了各催化剂在室温下对50mL、6%的H2O2溶液分解反应的催化作用情况.
[实验记录]各催化剂对50mL、6%的H2O2溶液分解反应的催化作用情况(室温22℃)
[实验分析]由表中数据及实验体验可以得出,MnO2催化分解H2O2制氧气有两点不足,①开始反应速率过快,氧气产生后,发生装置内压强骤然增大,使用分液漏斗滴液往往受阻,收集氧气排水或排空气时稍微耽搁,就会有不少O2逸失,到收集最后一瓶O2反应变慢,耗时太长.②______.
[提出问题]同学们认为用FeCl3溶液作催化剂效果最好.但FeCl3溶液为何能催化分解H2O2?
[实验猜想]已知FeCl3在水中可解离出Fe3+和Cl-,同学们提出以下猜想:
甲同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Cl-;
你认为最不可能的是______同学的猜想,理由是______.
同学们对余下的两个猜想,用实验进行了探究,请你仔细分析后填空:
[实验过程1]向盛有5mL、6%H2O2溶液的试管中加入少量的HCl溶液,并把带火星的木条伸入试管.
[实验现象1]无明显现象.对应结论:______.
[实验过程2]另向盛有5mL、6%的H2O2溶液的试管中加入少量的______,并再次把带火星的木条伸入试管.
[实验现象2]______.
对应结论:______.
[拓展研究]
同学们还比较了FeCl3和CuSO4两种盐对H2O2分解的催化效果,他们分成甲、乙两组,分别设计了如图一、图二所示的实验并进行了实验.(设两种盐溶液的浓度等条件相同)
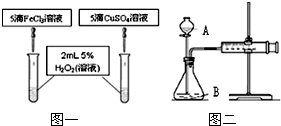
(1)指出仪器名称:A______B______
(2)写出以FeCl3为催化剂的反应的化学方程式______.
(3)图一可通过观察______来定性比较得出结论.有同学提出将药品CuSO4改为CuCl2更为合理,其理由是______,你认为药品还可以作何改进?______.
(4)检查图二装置气密性的方法是:______(填“打开”或“关闭”)仪器A的活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察到活塞又回到了原位,则说明装置气密性______(填“良好”或“不好”).该组同学利用图二所示实验需测量的数据是______(填序号:A.一定时间内收集到的气体体积B.收集一定体积的气体所需双氧水的质量).
研究小组还对溶液浓度、温度等实验条件进行了探究.下表选取了部分实验数据:
用足量等体积H2O2溶液制取相同体积O2所需的时间
[交流讨论]从上表中还能得出的结论是:______.

I、他们首先配制实验所需的50mL、6%的H2O2溶液.
[配制溶液]
现有一瓶新购置的双氧水,标签如图所示.
(1)若用这瓶双氧水来配置6%的医用双氧水1500g,需要这种双氧水的质量是多少克?
(2)另有一瓶5个月前购进的相同规格的双氧水,经检测,已缓慢分解放出了9.6g氧气,求现在剩余的该瓶溶液中溶质的质量分数.
II、然后同学们又比较了各催化剂在室温下对50mL、6%的H2O2溶液分解反应的催化作用情况.
[实验记录]各催化剂对50mL、6%的H2O2溶液分解反应的催化作用情况(室温22℃)
| 催化剂及用量 | O2平均产量 | 制氧所需时间 | 成本 | 反应情况 |
| MnO21.0g | 919mL | 10′03″ | 0.11元 | 分解先快后慢 |
| 10%FeCl3溶液5滴 | 985mL | 4′50″ | 0.02元 | 均匀产生O2 |
| 15%CuSO4溶液5滴 | 955mL | 4′57″ | 0.03元 | 均匀产生O2 |
[提出问题]同学们认为用FeCl3溶液作催化剂效果最好.但FeCl3溶液为何能催化分解H2O2?
[实验猜想]已知FeCl3在水中可解离出Fe3+和Cl-,同学们提出以下猜想:
甲同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Cl-;
你认为最不可能的是______同学的猜想,理由是______.
同学们对余下的两个猜想,用实验进行了探究,请你仔细分析后填空:
[实验过程1]向盛有5mL、6%H2O2溶液的试管中加入少量的HCl溶液,并把带火星的木条伸入试管.
[实验现象1]无明显现象.对应结论:______.
[实验过程2]另向盛有5mL、6%的H2O2溶液的试管中加入少量的______,并再次把带火星的木条伸入试管.
[实验现象2]______.
对应结论:______.
[拓展研究]
同学们还比较了FeCl3和CuSO4两种盐对H2O2分解的催化效果,他们分成甲、乙两组,分别设计了如图一、图二所示的实验并进行了实验.(设两种盐溶液的浓度等条件相同)

(1)指出仪器名称:A______B______
(2)写出以FeCl3为催化剂的反应的化学方程式______.
(3)图一可通过观察______来定性比较得出结论.有同学提出将药品CuSO4改为CuCl2更为合理,其理由是______,你认为药品还可以作何改进?______.
(4)检查图二装置气密性的方法是:______(填“打开”或“关闭”)仪器A的活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察到活塞又回到了原位,则说明装置气密性______(填“良好”或“不好”).该组同学利用图二所示实验需测量的数据是______(填序号:A.一定时间内收集到的气体体积B.收集一定体积的气体所需双氧水的质量).
研究小组还对溶液浓度、温度等实验条件进行了探究.下表选取了部分实验数据:
用足量等体积H2O2溶液制取相同体积O2所需的时间
| 浓度 时间(min) 条件 | 30%H2O2 | 15%H2O2 | 5%H2O2 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |

I、(1)设需要10%双氧水的质量是X,则X×10%=1500g×6% 解得:X=900g;
(2)设生成9.6g氧气需要过氧化氢的质量为Y,
2H2O2
2H2O+O2↑
68 32
Y9.6g
=
解得:Y=20.4g
现在剩余的该瓶溶液中溶质的质量分数为:
×100%=8.04%
II、[实验记录]由MnO2、FeCl3、CuSO4三种催化剂的用量及成本分析MnO2的缺点是:MnO2用量多,成本高;
[实验猜想]由过氧化氢溶液中含有水可知,最不可能的是甲同学的猜想,理由是过氧化氢溶液中有水;
[实验现象1]由向H2O2溶液的试管中加入少量的HCl溶液,不能使带火星的木条复燃可知,FeCl3溶液中的Cl-不能催化分解H2O2;
[实验过程2]为了验证Fe3+对H2O2的催化分解,另向盛有5mL、6%的H2O2溶液的试管中加入少量的Fe(NO3)3溶液;
[实验现象2]试管中有大量气泡产生,带火星的木条复燃;对应结论:起催化作用的是Fe3+;
[拓展研究]
(1)右图是可知标号仪器的名称是A是分液漏斗,B是锥形瓶;
(2)以FeCl3为催化剂的2H2O2分解反应的化学方程式是:2H2O2
2H2O+O2↑;
(3)由反应产生气泡快慢来比较催化效果,由于CuSO4和FeCl3的酸根不同;为了排除酸根离子的不同带来的干扰,可以将将FeCl3改为Fe2(SO4)3;
(4)由装置的特点及压强的变化可知,检查图二装置气密性的方法是:关闭仪器A的活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察到活塞又回到了原位,则说明装置气密性良好.该组同学利用图二所示实验需测量的数据是一定时间内收集到的气体体积;
[交流讨论]由表中的数据可知,H2O2溶液的质量分数越大产生氧气的速率越快.
故答为:I、[配制溶液](1)900g;(2)8.65%;II、[实验记录]MnO2用量多,成本高;[实验猜想]甲,过氧化氢溶液中有水;[实验现象1]FeCl3溶液中的Cl-不能催化分解H2O2;[实验过程2]Fe(NO3)3溶液;[实验现象2]试管中有大量气泡产生,带火星的木条复燃,起催化作用的是Fe3+;[拓展研究](1)分液漏斗,B是锥形瓶;
(2)2H2O2
2H2O+O2↑;(3)反应产生气泡快慢,使酸根相同,排除酸根的影响因素,将FeCl3改为Fe2(SO4)3;(4)关闭,良好,A;[交流讨论]H2O2溶液的质量分数越大产生氧气的速率越快.
(2)设生成9.6g氧气需要过氧化氢的质量为Y,
2H2O2
| ||
68 32
Y9.6g
| 68 |
| 32 |
| Y |
| 9.6g |
现在剩余的该瓶溶液中溶质的质量分数为:
| 1000g×10%-20.4g |
| 1000g-9.6g |
II、[实验记录]由MnO2、FeCl3、CuSO4三种催化剂的用量及成本分析MnO2的缺点是:MnO2用量多,成本高;
[实验猜想]由过氧化氢溶液中含有水可知,最不可能的是甲同学的猜想,理由是过氧化氢溶液中有水;
[实验现象1]由向H2O2溶液的试管中加入少量的HCl溶液,不能使带火星的木条复燃可知,FeCl3溶液中的Cl-不能催化分解H2O2;
[实验过程2]为了验证Fe3+对H2O2的催化分解,另向盛有5mL、6%的H2O2溶液的试管中加入少量的Fe(NO3)3溶液;
[实验现象2]试管中有大量气泡产生,带火星的木条复燃;对应结论:起催化作用的是Fe3+;
[拓展研究]
(1)右图是可知标号仪器的名称是A是分液漏斗,B是锥形瓶;
(2)以FeCl3为催化剂的2H2O2分解反应的化学方程式是:2H2O2
| ||
(3)由反应产生气泡快慢来比较催化效果,由于CuSO4和FeCl3的酸根不同;为了排除酸根离子的不同带来的干扰,可以将将FeCl3改为Fe2(SO4)3;
(4)由装置的特点及压强的变化可知,检查图二装置气密性的方法是:关闭仪器A的活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察到活塞又回到了原位,则说明装置气密性良好.该组同学利用图二所示实验需测量的数据是一定时间内收集到的气体体积;
[交流讨论]由表中的数据可知,H2O2溶液的质量分数越大产生氧气的速率越快.
故答为:I、[配制溶液](1)900g;(2)8.65%;II、[实验记录]MnO2用量多,成本高;[实验猜想]甲,过氧化氢溶液中有水;[实验现象1]FeCl3溶液中的Cl-不能催化分解H2O2;[实验过程2]Fe(NO3)3溶液;[实验现象2]试管中有大量气泡产生,带火星的木条复燃,起催化作用的是Fe3+;[拓展研究](1)分液漏斗,B是锥形瓶;
(2)2H2O2
| ||

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目

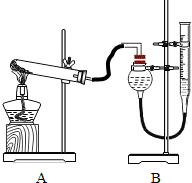 气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
气体为准,其它可能影响实验的因素均已忽略.相关数据见下表: