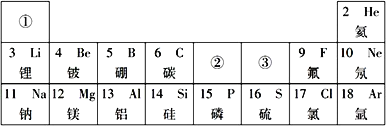
题目内容
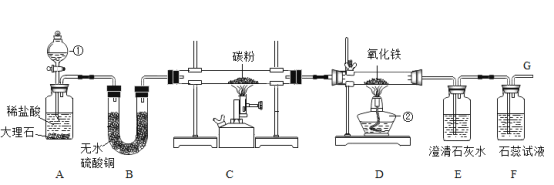
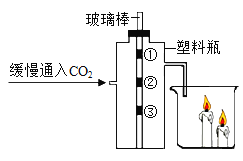
【题目】如图所示进行实验,①通入O2,点燃酒精灯,一段时间后,a中无明显现象,b中红磷燃烧:②立即改通N2,燃烧的红磷熄灭。下列叙述中错误的是
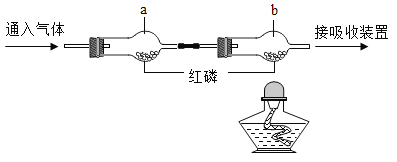
A.实验①说明可燃物燃烧需要氧气
B.实验②说明N2不支持燃烧
C.实验②可以改用CO2进行实验
D.实验①②对照可得出可燃物燃烧的条件
【答案】A
【解析】
燃烧的条件是物质是可燃物、温度达到可燃物的着火点、有氧气参与。
A、通入O2,点燃酒精灯,一段时间后,a中无明显现象,b中红磷燃烧,则实验①说明可燃物燃烧需要氧气、温度需要达到可燃物的着火点,故A不正确;
B、通入N2,点燃酒精灯,一段时间后,a、b中均无明显现象,说明氮气不能支持燃烧,实验②说明N2不支持燃烧,故B正确;
C、二氧化碳不能支持燃烧,可以采用二氧化碳进行实验,实验②可以改用CO2进行实验,故C正确;
D、实验①不加热,实验②加热,实验①②对照,能得出可燃物燃烧需要的条件,故D正确。故选A。

【题目】兴趣小组同学发现实验室一片久置的铜片表面附着有一层绿色固体,查阅资料得知绿色固体是铜绿[化学式为Cu2(OH)2CO3],甲同学从铜片上刮下一些铜绿进行如下探究,请填写下表中空白:
实验步骤 | 实验现象 | 实验结论 |
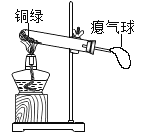
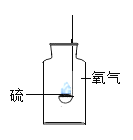
取少量铜绿在如图装置中加热
| 试管内壁有水珠。 | 铜绿加热产生_____。 |
_____ | 铜绿加热后生成氧化铜。 | |
气球胀大。 |
乙同学对实验结束装置冷却后气球胀大产生兴趣,于是进行了如下的探究:
(发现问题)气球为什么会胀大?
(提出猜想)
猜想I:试管内的空气受热膨胀使气球胀大;
猜想Ⅱ:铜绿加热产生二氧化碳使气球胀大;
猜想Ⅲ:铜绿加热产生一氧化碳使气球胀大;
猜想Ⅳ:铜绿加热产生一氧化碳和二氧化碳混合气体使气球胀大。
(实验与分析)
①小组经过讨论分析认为猜想_____不成立,理由是_____。
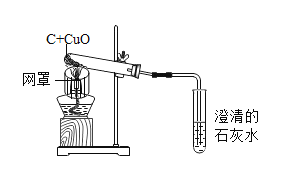
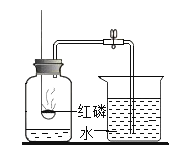
②乙同学用如图装置进行实验:
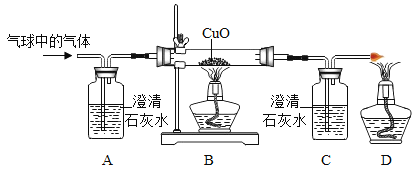
乙同学发现_____,说明铜绿加热后有CO2产生,产生此现象的化学方程式是_____,B处试管内的氧化铜没有变化,说明猜想_____不成立。
(实验结论)猜想Ⅱ成立。
(反思)加热铜绿反应的化学方程式是_____。
【题目】为了帮助同学们更好的理解空气中氧气含量测定的实验原理,老师利用传感器技术实时测定了实验装置图中图1内的压强、温度和氧气浓度,三条曲线变化如图2所示。

(1)X曲线表示的是_____(填“温度”或“氧气的浓度”)。
(2)结合X、Y两条曲线,解释图2中BC段气压变化的原因是_______。
(3)实验中测得的数据如下:
实验前 | 实验后 | ||
测量项目 | 烧杯中水的体积 | 烧杯中剩余水的体积 | 瓶中剩余气体的体积 |
体积/mL | 80.0 | 46.4 | 126.0 |
根据实验数据计算:测得的空气中氧气的体积分数为_____(列出计算式即可)。
(4)若测得的实验结果明显偏小,可能的原因是①______;②________。