题目内容
【题目】利用图甲装置探究“MnO2 的用量对 H2O2 分解反应的影响”,实验中 H2O2 的溶质质量分 数为 3%,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内 压强成正比。反应放热忽略不计)
(1)写出装置中发生反应的文字或符号表达式:___,MnO2 在此反应前后___和__不发生改变。
(2)图乙是“0.1 克 MnO2 不同体积的 3% H2O2 溶液混合”的实验结果,从图中可以看______。
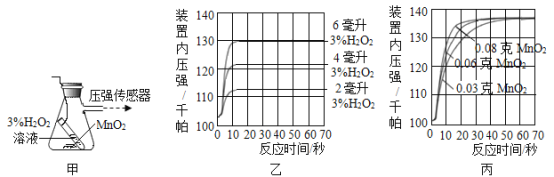
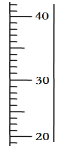
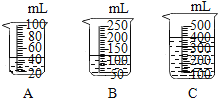
(3)当用“3% H2O2 溶液 8 毫升与不同质量的 MnO2 混合”时,得到如图丙所示的曲线。曲线的斜率显示,当 MnO2 的用量增加到 0.08 克时,分解速度达到实验要求。 在此实验条件下,若 MnO2 的质量有 4 克(一药匙),就能使如图_____(选填字母)烧杯 中所装的 3% H2O2 溶液,其分解速度最接近实验要求。
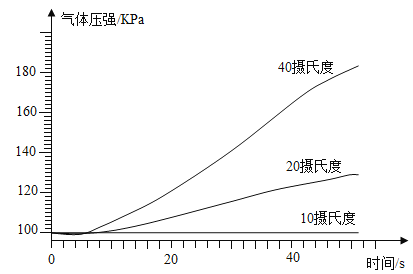
(4)使用压强传感器等设备,检测不同温度下过氧化氢分解时气体压强的变化。经过实验、数据处理等,获得如右图所示的压强-时间的曲线变化。由此可知,其它条件一定时,温度越高,过氧化氢的分解速率______(填 “越快”、“越 慢”或“不变”);
(5)请你设计实验方案,探究浓度对过氧化氢分解速率的影响(写出简要的实验步骤)______。
【答案】H2O2![]() H2O+O2质量化学性质过氧化氢体积越大,分解产生的氧气越多C越快在两支试管中分别加入 10mL5%和 10%的过氧化氢溶液,同时分别加入少量等量的二氧化锰,观察两支试管中产生气体的快慢。
H2O+O2质量化学性质过氧化氢体积越大,分解产生的氧气越多C越快在两支试管中分别加入 10mL5%和 10%的过氧化氢溶液,同时分别加入少量等量的二氧化锰,观察两支试管中产生气体的快慢。
【解析】
(1) 过氧化氢在二氧化锰的催化作用下生成水和氧气,符号表达式为:H2O2![]() H2O+O2;二氧化锰是催化剂,在此反应前后质量和化学性质不发生改变;
H2O+O2;二氧化锰是催化剂,在此反应前后质量和化学性质不发生改变;
(2)根据图示可以看出其他条件相同时,H2O2的用量越多,产生的氧气越多;
(3)由图示可知3%H2O2溶液8毫升与0.08克MnO2混合,分解速度达到实验要求,若MnO2的质量有4克需要3%H2O2溶液=![]() ×8mL=400mL
×8mL=400mL
(4)过氧化氢分解生成水和氧气,生成的氧气越多,压强越大,由不同温度下过氧化氢分解时气体压强如图所示的压强-时间的曲线变化,其它条件一定时,温度越高,气体的压强越大,说明过氧化氢的分解速率越快;
(5)过氧化氢溶液分解还受到过氧化氢浓度的影响,可根据控制变量法,控制其它条件相同,在两支试管中分别加入10mL5%和10%的过氧化氢溶液,同时分别加入少量等质量的二氧化锰,观察两支试管中产生气体的快慢(其它合理即可)。

【题目】用来测定空气成分的方法很多,如图所示的是小明用红磷在空气中燃烧的测定方法。实验过程是:

第一步:将集气瓶容积划分为五等份,并做好标记。
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧。
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5。
请回答下列问题:
(1)实验过程中,观察到的主要现象是____________,反应的文字表达式是__________。
(2)上面的实验同时证明了氮气有_________的化学性质。
(3)实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果的原因可能是_______________。
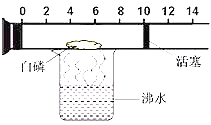
(4)拓展:上图是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方,进行实验。请完成实验报告:
实验目的 | 实验现象 | 实验结论 |
测定空气中______的体积分数 | 白磷着火燃烧,活塞先右移,后左移,最后停在刻度约为_______(填整数)的位置上。 | 空气的成分按体积计算,________约占21% |
【题目】某校兴趣小组在实验室中完成制取氧气的实验。他们取氯酸钾和二氧化锰的混合物共6g放入大试管中加热,并在同时测定试管中剩余固体物质的质量(如下表),
请分析表中数据,完成下列问题:
反应时间/min | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
剩余固体质量/g | 5.20 | 4.60 | 4.20 | 4.10 | 4.08 |
(1)完全反应时,生成氧气的质量为_____g;
(2)原混合物中氯酸钾的质量分数是__________?(计算结果精确到0.1%)