题目内容
某实验小组的同学用下图三个装置验证质量守恒定律,其中,不能达到实验目的是________(填字母),理由是________.A中的实验现象是________.C中发生反应的化学方程式是________.
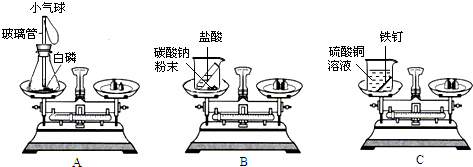
B 生成的气体逸出或没有在密闭容器中进行反应 气球体积变小 CuSO4+Fe═FeSO4+Cu
分析:根据质量守恒定律可知,化学反应前后各种物质的质量之和相等.如果天平一直保持平衡,说明反应前后质量不变.因此有气体参加或者有气体生成的反应一定要密封,防止气体出去;没有气体的反应则不用密封.
解答:根据质量守恒定律可知,化学反应前后各种物质的质量之和相等.如果天平一直保持平衡,说明反应前后质量不变.因此有气体参加或者有气体生成的反应一定要密封,防止气体出去;没有气体的反应则不用密封.白磷的着火点很低,白磷会自然,由于氧气参加反应,所以随着氧气的减少,气体的体积也会变小.碳酸钠和稀盐酸反应生成氯化钠和水和二氧化碳,二氧化碳气体会进入大气中.硫酸铜和铁生成硫酸亚铁和铜.
故答案为:B;生成的气体逸出或没有在密闭容器中进行反应;气球体积变小;CuSO4+Fe═FeSO4+Cu.
点评:理解质量守恒定律的内涵,如果天平一直保持平衡,说明反应前后质量不变.因此有气体参加或者有气体生成的反应一定要密封,防止气体出去;没有气体的反应则不用密封.
分析:根据质量守恒定律可知,化学反应前后各种物质的质量之和相等.如果天平一直保持平衡,说明反应前后质量不变.因此有气体参加或者有气体生成的反应一定要密封,防止气体出去;没有气体的反应则不用密封.
解答:根据质量守恒定律可知,化学反应前后各种物质的质量之和相等.如果天平一直保持平衡,说明反应前后质量不变.因此有气体参加或者有气体生成的反应一定要密封,防止气体出去;没有气体的反应则不用密封.白磷的着火点很低,白磷会自然,由于氧气参加反应,所以随着氧气的减少,气体的体积也会变小.碳酸钠和稀盐酸反应生成氯化钠和水和二氧化碳,二氧化碳气体会进入大气中.硫酸铜和铁生成硫酸亚铁和铜.
故答案为:B;生成的气体逸出或没有在密闭容器中进行反应;气球体积变小;CuSO4+Fe═FeSO4+Cu.
点评:理解质量守恒定律的内涵,如果天平一直保持平衡,说明反应前后质量不变.因此有气体参加或者有气体生成的反应一定要密封,防止气体出去;没有气体的反应则不用密封.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案
相关题目
被称为“生命之源”的水(H2O)和被称为“绿色氧化剂”的过氧化氢(H2O2),都是由氢、氧两种元素组成的化合物,通常情况下均为无色液体.某实验小组的同学用下面的方法鉴别水和双氧水两瓶无色液体:
(1)请填写上表中有关内容:
(2)写出B试管中发生反应的文字表达式: .
| 实验步骤 | 实验现象 | 实验结论 |
①将等体积的两种无色液体分别加入A、B两个试管中.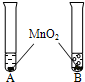 ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象. ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象. |
A试管中无明显现象 B试管中有气泡 产生 |
A试管中的无色液 体是 B试管中的无色液体是 |
(2)写出B试管中发生反应的文字表达式:
被称为“生命之源”的水(H2O)和被称为“绿色氧化剂”的过氧化氢(H2O2),都是由氢、氧两种元素组成的化合物,通常情况下均为无色液体.某实验小组的同学用下面的方法鉴别水和双氧水两瓶无色液体.请回答有关问题:
填写上表有关内容.写出B试管中发生反应的文字表达式______

| 实验步骤 | 实验现象 | 实验结论 |
| ①将等体积的两种无色液体分别加入A、B两个试管中. ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象. | B试管中有气泡产生 | A试管中的无色液体是______. |

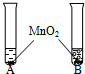
 被称为“生命之源”的水(H2O)和被称为“绿色氧化剂”的过氧化氢(H2O2),都是由氢、氧两种元素组成的化合物,通常情况下均为无色液体.某实验小组的同学用下面的方法鉴别水和双氧水两瓶无色液体.请回答有关问题:
被称为“生命之源”的水(H2O)和被称为“绿色氧化剂”的过氧化氢(H2O2),都是由氢、氧两种元素组成的化合物,通常情况下均为无色液体.某实验小组的同学用下面的方法鉴别水和双氧水两瓶无色液体.请回答有关问题: