题目内容
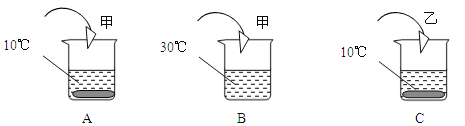
【题目】(4分)A、B、C三个烧杯中都盛有40g水(其中A、C烧杯中水温为10℃,B烧杯中水温为30℃,不考虑溶解过程中温度的变化),分别加入甲、乙(均不含结晶水)两物质各10g,充分搅拌后所得现象如下图所示,试回答:
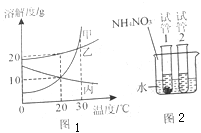
已知:甲、乙的溶解度随温度的变化如图所示
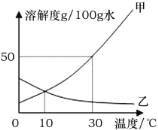
(1)若要将B烧杯中的溶液变为饱和溶液,还需要加入物质甲__________克。
(2)其它条件不变,将C烧杯中的温度升到50℃时,C烧杯中的溶液是__________(填“饱和”或“不饱和”)溶液。
(3)10℃时,以上A、C烧杯中的溶液质量分数关系为A__________C(填“=”或“>”、“<”,下同)。若其他条件
不变,将温度升高,则A、C烧杯中的溶液质量分数关系为A__________C。
【答案】(1)10g (2)饱和 (3)= >
【解析】
试题分析:(1)由图可知,30℃时,甲的溶解度为50g,所以应再加入10g 甲才能 将B烧杯中的溶液变为饱和溶液 (2)其它条件不变,将C烧杯中的温度升到50℃时,乙的溶解度变小,小于40g,C烧杯中的溶液是饱和溶液。(3)10℃时,A、C的溶解度相同,烧杯中的溶液都达到饱和,溶质的质量分数相同,若其他条件不变,将温度升高,则A的溶质至两份苏不变,C的溶液质量分数减小,A、C烧杯中的溶液质量分数关系为A>C

练习册系列答案
相关题目