题目内容
【题目】某水溶液中含有以下离子中的若干种:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,现取两份100ml溶液进行如下实验:
,现取两份100ml溶液进行如下实验:
(1)第一份加入![]() 溶液有沉淀产生。
溶液有沉淀产生。
(2)第二份加足量![]() 溶液后,得沉淀物6.27g,经足量硝酸洗涤、干燥后,沉淀质量为2.33g,在所得滤液中加入
溶液后,得沉淀物6.27g,经足量硝酸洗涤、干燥后,沉淀质量为2.33g,在所得滤液中加入![]() 溶液有沉淀产生。根据上述实验,以下推测正确的是( )
溶液有沉淀产生。根据上述实验,以下推测正确的是( )![]()
A.![]() 一定存在B.100mL溶液中
一定存在B.100mL溶液中![]() 的质量不小于2.34g
的质量不小于2.34g
C.![]() 一定不存在D.
一定不存在D.![]() 一定不存在,
一定不存在,![]() 可能存在
可能存在
【答案】B
【解析】
由题意第一份溶液中加入![]() 溶液有沉淀产生,说明溶液中可能含有氯离子、碳酸根离子或硫酸根离子;第二份溶液加入氯化钡溶液,得沉淀物,经足量硝酸洗涤、干燥后,沉淀质量减少,说明加入氯化钡后产生两种沉淀,因此溶液中一定含有碳酸根离子和硫酸根离子,因为镁离子、钡离子能与碳酸根离子结合成沉淀,因此溶液中一定不含镁离子和钡离子。溶液中阴阳离子的电荷守恒,溶液中的阳离子只有钾离子,因此一定含有钾离子,因为氯化钡中含有氯离子,所以不能确定原溶液是否含有氯离子。要判断钾离子的质量,则需要利用硫酸钾与氯化钡反应、碳酸钾与氯化钡反应的化学方程式来进行计算,上述反应中已知生成物硫酸钡和碳酸钡的质量。
溶液有沉淀产生,说明溶液中可能含有氯离子、碳酸根离子或硫酸根离子;第二份溶液加入氯化钡溶液,得沉淀物,经足量硝酸洗涤、干燥后,沉淀质量减少,说明加入氯化钡后产生两种沉淀,因此溶液中一定含有碳酸根离子和硫酸根离子,因为镁离子、钡离子能与碳酸根离子结合成沉淀,因此溶液中一定不含镁离子和钡离子。溶液中阴阳离子的电荷守恒,溶液中的阳离子只有钾离子,因此一定含有钾离子,因为氯化钡中含有氯离子,所以不能确定原溶液是否含有氯离子。要判断钾离子的质量,则需要利用硫酸钾与氯化钡反应、碳酸钾与氯化钡反应的化学方程式来进行计算,上述反应中已知生成物硫酸钡和碳酸钡的质量。
由题意第一份溶液中加入![]() 溶液有沉淀产生,说明溶液中可能含有氯离子、碳酸根离子或硫酸根离子;第二份溶液加入氯化钡溶液,得沉淀物,经足量硝酸洗涤、干燥后,沉淀质量减少,说明加入氯化钡后产生两种沉淀,因此溶液中一定含有碳酸根离子和硫酸根离子,因为镁离子、钡离子能与碳酸根离子结合成沉淀,因此溶液中一定不含镁离子和钡离子。溶液中阴阳离子的电荷守恒,溶液中的阳离子只有钾离子,因此一定含有钾离子,不能确定是否含有氯离子。则:
溶液有沉淀产生,说明溶液中可能含有氯离子、碳酸根离子或硫酸根离子;第二份溶液加入氯化钡溶液,得沉淀物,经足量硝酸洗涤、干燥后,沉淀质量减少,说明加入氯化钡后产生两种沉淀,因此溶液中一定含有碳酸根离子和硫酸根离子,因为镁离子、钡离子能与碳酸根离子结合成沉淀,因此溶液中一定不含镁离子和钡离子。溶液中阴阳离子的电荷守恒,溶液中的阳离子只有钾离子,因此一定含有钾离子,不能确定是否含有氯离子。则:
A、![]() 一定存在,A选项错误,不符合题意;
一定存在,A选项错误,不符合题意;
B、第二份加足量![]() 溶液后,得沉淀物6.27g,经足量硝酸洗涤、干燥后,沉淀质量为2.33g,则硫酸钡的质量为2.33g,碳酸钡的质量为
溶液后,得沉淀物6.27g,经足量硝酸洗涤、干燥后,沉淀质量为2.33g,则硫酸钡的质量为2.33g,碳酸钡的质量为![]() ,设硫酸钾与氯化钡反应生成的氯化钾的质量为x,碳酸钾与与氯化钡反应生成的氯化钾的质量为y,则有:
,设硫酸钾与氯化钡反应生成的氯化钾的质量为x,碳酸钾与与氯化钡反应生成的氯化钾的质量为y,则有:
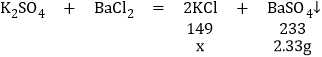
由![]() 解得x=1.49g
解得x=1.49g
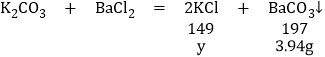
由![]() 解得y=2.98g
解得y=2.98g
生成的氯化钾的质量为![]() ;
;
4.47g氯化钾中钾元素的质量为![]() ;
;
由于不确定是否含有氯离子,根据钾元素守恒,100mL溶液中![]() 的质量不小于2.34g,B选项正确,符合题意;
的质量不小于2.34g,B选项正确,符合题意;
C、![]() 一定不存在,C选项错误,不符合题意;
一定不存在,C选项错误,不符合题意;
D、![]() 一定不存在,
一定不存在,![]() 一定不存在,D选项错误,不符合题意。故选B。
一定不存在,D选项错误,不符合题意。故选B。

【题目】I、某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成。实验小组欲探究该水垢的主要成分:
(猜想与分析)分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是:
①CaO ②Ca(OH)2 ③CaCO3 ④Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是___
(实验与事实)
实验一 | 实验现象 | 解释或结论 | ||
将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | 不变色说明水垢中一定没有___ | ||
实验二 | 实验现象 | 解释或结论 | ||
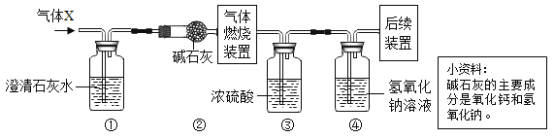
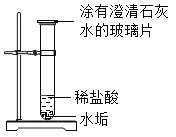
| 反应一段时间后水垢消失,溶液澄清;玻璃片上澄清石灰水变浑浊 | 石灰水变浑浊,说明有CO2生成。则水垢中一定含有_____ | ||
(原理与呈现)请用化学方程式表示实验二中有关反应的化学反应原理:
(1)____,(2)________。
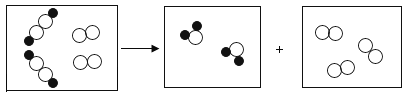
II、在探究金属活动性的实验课上,同学们把打磨光亮的铝片插入硫酸铜溶液中,过一会儿,发现了一个“意外现象”:在铝片表面看到有红色固体析出的同时,还看到有少量的气泡冒出,写出生成红色固体的化学方程式____.
(提出问题)该气体是什么呢?
(猜想与假设)猜想一:O2 猜想二:H2 猜想三:CO2 猜想四:SO2
同学们经过讨论,一致认为猜想三不成立,理由是___.
(实验验证)⑴有同学闻了一下该气体,发现无气味,证明猜想四也不成立,理由是___.
⑵将产生的气体经验纯后,用导管导入到点燃的酒精灯火焰上,气体安静燃烧,产生淡蓝色火焰.
(实验结论)____.
(反思与交流)CuSO4溶液可能显____性(填“酸”或“碱”或“中”).