题目内容
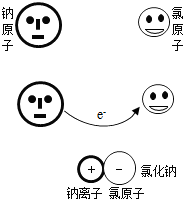 微粒模型观察与比较.如右图所示,在钠与氯气的反应中,每个钠原子失去1个电子,成为1个钠离子;每个氯原子得到1个电子,成为1个氯离子;钠离子与氯离子结合形成氯化钠.因为1个电子的质量大约为1个质子或中子质量的
微粒模型观察与比较.如右图所示,在钠与氯气的反应中,每个钠原子失去1个电子,成为1个钠离子;每个氯原子得到1个电子,成为1个氯离子;钠离子与氯离子结合形成氯化钠.因为1个电子的质量大约为1个质子或中子质量的| 1 | 1836 |
(1)请你画出微粒结构示意图Na+;Cl
(2)若用r、m分别表示微粒的半径和质量,以“<”或“>”或“≈”填空.
①m(Na)
③r(Na)
分析:本题考查原子和离子的相互转化.
(1)在化学反应中,金属原子最外层电子少于4个,易失去电子,达到8个电子的稳定结构,非金属原子最外层电子多于4个,易得到电子,达到8个电子的稳定结构.
(2)电子的质量很小,几乎可忽略,比较半径时,先看电子层,层越多,半径越大,相同的电子层时,看质子数,质子数越大,半径越小.
(1)在化学反应中,金属原子最外层电子少于4个,易失去电子,达到8个电子的稳定结构,非金属原子最外层电子多于4个,易得到电子,达到8个电子的稳定结构.
(2)电子的质量很小,几乎可忽略,比较半径时,先看电子层,层越多,半径越大,相同的电子层时,看质子数,质子数越大,半径越小.
解答:解:(1)在化学反应中,金属失去电子,在原子中,电子在核外分层排布,每层最多填2n2个电子,最外层不超过8个,故答案为
 .
.
(2)①一个电子的质量很小,钠原子的质量与钠离子的质量可认为接近相等,故答案为:≈.
②氯离子和氯原子相比,得到了电子,使半径变大,故答案为:<.
③相同的电子层时,质子数越大,半径越小,氯的质子数大,则半径小,故答案为:>.
④电子层越多,半径越大,故答案为:<.

 .
.(2)①一个电子的质量很小,钠原子的质量与钠离子的质量可认为接近相等,故答案为:≈.
②氯离子和氯原子相比,得到了电子,使半径变大,故答案为:<.
③相同的电子层时,质子数越大,半径越小,氯的质子数大,则半径小,故答案为:>.
④电子层越多,半径越大,故答案为:<.
点评:应熟悉电子的排布,明确最外层电子从而理解其在化学反应中的性质,归纳比较微粒半径的一般方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
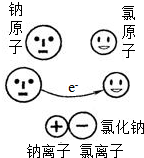 微粒模型观察与比较.如下图所示,在钠与氯气的反应中,每个钠原子失去1个电子,成为1个钠离子;每个氯原子得到1个电子,成为1个氯离子;钠离子与氯离子结合形成氯化钠.因为1个电子的质量大约为1个质子或中子质量的
微粒模型观察与比较.如下图所示,在钠与氯气的反应中,每个钠原子失去1个电子,成为1个钠离子;每个氯原子得到1个电子,成为1个氯离子;钠离子与氯离子结合形成氯化钠.因为1个电子的质量大约为1个质子或中子质量的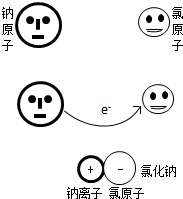
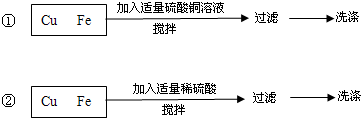
 ,故原子的质量几乎都集中在原子核上。
,故原子的质量几乎都集中在原子核上。 别表示微粒的半径和质量,以“<”或“>”或“≈”填空。
别表示微粒的半径和质量,以“<”或“>”或“≈”填空。
 ▲ r(Cl-);
▲ r(Cl-); ,故原子的质量几乎都集中在原子核上.
,故原子的质量几乎都集中在原子核上.