题目内容
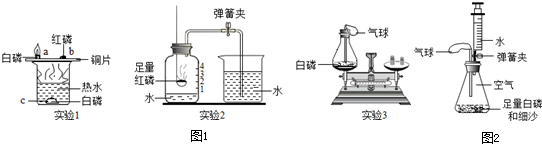
(6分)白磷、红磷都是可燃物,都可以在一定条件下燃烧。以下是利用它们的可燃性进行的三个实验,请分别回答问题。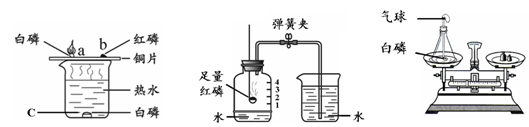
实验1 实验2 实验3
(1)通过实验1可以探究燃烧的条件。烧杯中放有热水,a、b、c处分别放有药品,实验中只有a处的白磷燃烧。a与c对比、a与b对比,说明燃烧需要的条件是可燃物与氧气接触和 ,白磷燃烧的化学方程式为 。
(2)通过实验2可以测定 。待集气瓶中的红磷熄灭,冷却后打开弹簧夹,当观察到 的现象时,可达到该实验目的。
(3)通过实验3可以验证质量守恒定律。实验前将白磷放入锥形瓶中,称量装置的总质量,引燃白磷,待反应后再称量装置总质量,发现托盘天平保持平衡。整个实验过程中气球会出现的现象是 。
综合分析上述三个实验,以下说法正确的是 。(填①~⑥序号)
①实验1中的热水只起隔绝空气的作用
②实验2中红磷可以换成木炭
③实验2若未达到实验目的,可能是由于装置气密性不好
④实验2中两容器中水所起的作用相同
⑤实验3中的气球起到了防止锥形瓶内的烟气与外界交换的作用
⑥实验3锥形瓶内事先放少量细沙的作用是防止瓶底炸裂
(1)温度达到着火点 4P + 5O2 2P2O5
2P2O5
(2)空气中氧气含量 烧杯中的水进入集气瓶中,液面约上升到刻度1处
(3)气球先膨胀后缩小 ③⑤⑥
解析试题分析:(1)根据燃烧的条件分析,燃烧需要同时满足三个条件,即可燃物、与氧气接触、温度达到着火点及以上;白磷在空气中燃烧,生成五氧化二磷,故反应的化学方程式为4P + 5O2 2P2O5。
2P2O5。
(2)实验2可以用来测定空气中氧气的含量,实验是利用足量红磷的燃烧来消耗集气瓶中的空气中的氧气,使瓶内压强减小,当集气瓶中的红磷熄灭,冷却后打开弹簧夹时,烧杯中的水会进入集气瓶中,且进入水的体积就是消耗氧气的体积,由于氧气约占空气总体积的1/5 ,故最终液面会约上升到刻度1处。
(3)由于锥形瓶中白磷燃烧会放出热量,会使瓶内气体急剧膨胀,所以气球膨胀,但燃烧熄灭后,冷却到室温时,由于白磷燃烧消耗了瓶内氧气,故瓶内气体减少,压强减小,所以气球又会变小。
根据以上三个实验分析。
①实验1中的热水不仅起隔绝空气的作用,还起到加热的作用,错误;
②实验2中红磷不能换成木炭,因为木炭燃烧生成的是二氧化碳气体,不能改变集气瓶内的压强,故不能达到实验的目的,错误;
③实验2中若装置气密性不好,会达不到实验的目的,正确;
④实验2中的两容器中水所起的作用本同,集气瓶中的少量水是用来吸收生成的五氧化二磷的,防止其污染空气,烧杯中的水是用来测定空气中氧气的体积的,错误
⑤实验3中,由于反应过程中有压强的改变,故气球起到了平衡瓶内外气体压强的作用,也就避免了锥形瓶内的烟气与外界的交换,正确;
⑥实验3中,锥形瓶内事先放少量细沙的作用是防止瓶底过热而炸裂,正确。故选③⑤⑥
考点:燃烧的条件与灭火原理探究,测定空气里氧气含量的探究,质量守恒定律的实验探究
点评:本题是对课本实验的考查,化学是以实验为基础的学科,故理解实验的原理,熟练掌握实验的操作、现象、以及注意事项等,是解答本题的关键。

 快捷英语周周练系列答案
快捷英语周周练系列答案 27、科学探究常用控制实验条件(控制变量)进行对比实验的方法.如关于燃烧条件的探究有:可燃物、助燃物、着火点(温度)三个控制变量.
27、科学探究常用控制实验条件(控制变量)进行对比实验的方法.如关于燃烧条件的探究有:可燃物、助燃物、着火点(温度)三个控制变量.
 27、科学探究常用控制实验条件(控制变量)进行对比实验的方法.如关于燃烧条件的探究有:可燃物、助燃物、着火点(温度)三个控制变量.
27、科学探究常用控制实验条件(控制变量)进行对比实验的方法.如关于燃烧条件的探究有:可燃物、助燃物、着火点(温度)三个控制变量.