题目内容
【题目】构建知识网络,可以帮助理解知识间的内在联系。下图是盐酸与不同类别物质之间反应的知识网络。(由金属离子和酸根离子组成的化合物叫做盐,如CuSO4)
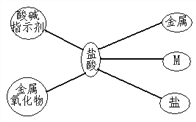
⑴图中M应为______类物质;
⑵写出一种能与盐酸反应的盐________(写化学式) ;
⑶用盐酸除铁锈(主要成分Fe2O3)的化学方程式_______________________。
【答案】 碱 CaCO3 Fe2O3+6HCl==2FeCl3+3H2O
【解析】本题考查了酸的化学性质,熟悉酸的通性理解题的关键。
(1)盐酸可与酸碱指示剂、碱、金属、金属氧化物、某些盐发生化学反应,图中M应为其中的碱类物质;
(2)碳酸钙是由碳酸根离子和钠离子组成化合物属于盐,碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,所以答案为:CaCO3;
⑶铁锈主要成分是氧化铁,属于金属氧化物,与盐酸反应生成盐和水,反应中元素的化合价不变,其方程式为:Fe2O3+6HCl==2FeCl3+3H2O。

【题目】某校化学研究性学习课题组的同学们为了测定某氢氧化钙样品中Ca (OH)2含量(含有的杂质为CaCO3),共做了3次实验,使一定质量的该样品分别与同一种盐酸反应,所得相关实验数据记录如下表:
第1次 | 第2次 | 第3次 | |
所取样品的质量 | 20g | 20g | 20g |
所取稀盐酸的质量 | 80g | 100g | 120g |
生成CO2的质量 | 3.58g | 4.4g | 4.4g |
(1)在第 次实验中,反应容器内有白色固体剩余。
(2)求原样品中Ca(OH)2的质量分数?
【题目】20℃时,NaCl溶解情况见下表,相关叙述正确的是
实验 序号 | 水的 质量(g) | 加入NaCl 的质量(g) | 溶液的 质量(g) |
① | 10.0 | 1.5 | 11.5 |
② | 10.0 | 3.0 | 13.0 |
③ | 10.0 | 4.5 | 13.6 |
④ | 10.0 | 6.0 | 13.6 |
A. ①所得溶液的溶质质量分数为15.0%
B. ②中所得溶液是饱和溶液
C. 20℃时,NaCl 的溶解度是45.0g/100g 水
D. ③④溶液的溶质质量分数相等