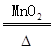题目内容
【题目】将干燥的氯酸钾与二氧化锰混合固体8g放到大试管中加热,反应完全后,冷却到反应前的温度,称量得剩余固体的质量为5.6g.求原混合物中二氧化锰的质量分数是多少?(保留一位小数)
【答案】解:利用质量守恒定律,由反应前后固体物质的质量差待反应至不再有气体生成后,制取氧气的质量=8g﹣5.6g=2.4g
设完全反应时消耗氯酸钾的质量为x
2KClO3 |
| 2KCl | + | 3O2↑ |
245 | 96 | |||
x | 2.4g |
![]()
x=6.125g
二氧化锰在剩余固体中的质量分数= ![]() ×100%=23.4%.
×100%=23.4%.
给答案为:23.4%
【解析】加热氯酸钾和二氧化锰的混合物,氯酸钾受热分解生成氯化钾和氧气,二氧化锰在变化过程中为催化剂,反应前后质量和化学性质都不变;利用质量守恒定律,由反应前后固体物质的质量差,可求得放出气体氧气的质量;根据反应的化学方程式,利用生成氧气的质量可计算原混合物中氯酸钾的质量;根据反应后二氧化锰的质量不变可计算其质量分数.
【考点精析】解答此题的关键在于理解根据化学反应方程式的计算的相关知识,掌握各物质间质量比=系数×相对分子质量之比.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】空气在标准状况下的密度是1.29g/L,以下四种气体中既能用排水法收集,又能用向下排空气法收集的是( )
气 体 | A | B | C | D |
标准状况下密度/(g.L﹣1) | 1.997 | 1.429 | 0.771 | 0.717 |
溶 解 性 | 可溶 | 微溶 | 易溶 | 难溶 |
A.A
B.B
C.C
D.D