题目内容
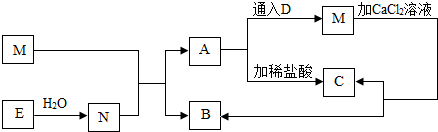
现有一固体混合物A,其中可能含有氧化铁、铜、碳酸铵、氯化钙四种物质中的两种或多种,按如图所示进行实验,出现的现象如图中所述(假设所有可能发生的反应均恰好完全反应),试用化学式回答下列问题:
(1)气体D是
(2)物质A中不能确定的物质是
(3)溶液G中一定含有的溶质是 、
(4)C→F的化学方程式为 .

(1)气体D是
(2)物质A中不能确定的物质是
(3)溶液G中一定含有的溶质是
(4)C→F的化学方程式为
考点:物质的鉴别、推断,盐的化学性质,化学式的书写及意义
专题:混合物组成的推断题
分析:根据氧化铁、铜难溶于水,碳酸根离子和钙离子会生成碳酸钙沉淀,碳酸钙和盐酸反应会生成二氧化碳气体,铜和盐酸不会反应,氧化铁和盐酸会生成氯化铁和水等知识进行分析.
解答:解:氧化铁、铜难溶于水,碳酸根离子和钙离子会生成碳酸钙沉淀,碳酸钙和盐酸反应会生成二氧化碳气体,铜和盐酸不会反应,氧化铁和盐酸会生成氯化铁和水.
固体混合物A加水溶解后,得到滤液B和沉淀C,滤液B中加入氢氧化钠会生成气体D和溶液E,所以滤液B中含有铵根离子,所以A中一定含有碳酸铵,沉淀C和盐酸反应会生成气体,所以沉淀C中一定含有碳酸钙沉淀,所以A中一定含有氯化钙,沉淀C中加入过量的盐酸后,还有沉淀H,所以H是铜,所以A中也一定含有铜,氧化铁和盐酸会生成氯化铁和水,氯化铁溶于水,无法判断溶液G的成分,所以不能确定A中是否含有氧化铁,所以
(1)通过推导可知:气体D是:NH3;
(2)氧化铁和盐酸会生成氯化铁和水,氯化铁溶于水,无法判断溶液G的成分,所以不能确定A中是否含有氧化铁,所以物质A中不能确定的物质是:Fe2O3;
(3)通过推导可知,沉淀C是碳酸钙、铜与过量的盐酸反应后,溶液G中含有生成的氯化钙和未反应完的盐酸,所以溶液G中一定含有的溶质是:CaCl2,HCl;
(4)C→F的反应是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答案为:(1)NH3;
(2)Fe2O3;
(3)CaCl2,HCl;
(4)CaCO3+2HCl=CaCl2+H2O+CO2↑.
固体混合物A加水溶解后,得到滤液B和沉淀C,滤液B中加入氢氧化钠会生成气体D和溶液E,所以滤液B中含有铵根离子,所以A中一定含有碳酸铵,沉淀C和盐酸反应会生成气体,所以沉淀C中一定含有碳酸钙沉淀,所以A中一定含有氯化钙,沉淀C中加入过量的盐酸后,还有沉淀H,所以H是铜,所以A中也一定含有铜,氧化铁和盐酸会生成氯化铁和水,氯化铁溶于水,无法判断溶液G的成分,所以不能确定A中是否含有氧化铁,所以
(1)通过推导可知:气体D是:NH3;
(2)氧化铁和盐酸会生成氯化铁和水,氯化铁溶于水,无法判断溶液G的成分,所以不能确定A中是否含有氧化铁,所以物质A中不能确定的物质是:Fe2O3;
(3)通过推导可知,沉淀C是碳酸钙、铜与过量的盐酸反应后,溶液G中含有生成的氯化钙和未反应完的盐酸,所以溶液G中一定含有的溶质是:CaCl2,HCl;
(4)C→F的反应是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答案为:(1)NH3;
(2)Fe2O3;
(3)CaCl2,HCl;
(4)CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评:在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
钠原子与钠离子在结构上相同的是( )
| A、核电荷数 | B、质子数 |
| C、电子层数 | D、电子数 |
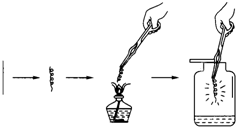 某实验小组做铁丝在氧气中燃烧实验,如图所示,试回答:
某实验小组做铁丝在氧气中燃烧实验,如图所示,试回答: