题目内容
【题目】下图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
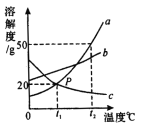
(1)t2℃时30ga物质加入到50g水中不断搅拌,能形成80g溶液吗? (填写“能”或“不能”)。
(2)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是 (填写物质序号)。
(3)将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是 (填写序号)
A.c>a=b B.a=b>c C.a>b>c D.b>a>c
【答案】(1)不能 (2)c<b<a(或cba) (3)D
【解析】
试题分析:(1)根据溶解度曲线, t2℃时,a物质的溶解度为50g,故将100 g a物质加入到100 g水中并充分搅拌,只能溶解50g,故在50g水中最多只能溶解25g,故只能形成75g溶液,故不能
(2)根据溶解度曲线,t2℃时a、b、c三种物质的溶解度按由小到大的顺序:c<b<a(或cba)
(3)根据溶解度曲线,物质a、b的溶解度都随温度的升高而增大,故将t10C时a、b两种物质的饱和溶液分别升温到t20C时,都由t10C时的饱和溶液变为t20C时的不饱和溶液,但溶液中的溶质、溶剂质量不变,故溶质质量分数也不变,而在t10C 时:b的溶解度大于a,故溶质质量分数b也大于a,而对于c而言,溶解度随温度的升高而降低,故t10C升温到t20C,有晶体析出,溶液中的溶质质量减少,故溶质质量分数也减小,成为t20C时的饱和溶液,而在t20C时,物质c的溶解度要小于t10C时a的溶解度,故c的溶质质量分数最小,故若将t10C三种物质的饱和溶液分别升温到t20C时,则三种溶液中溶质的质量分数大小关系是:b>a>c

【题目】(18分)实验室处理一批过期的化学药品,兴趣小组同学决定对一癣已经结块的氢氧化钠样品展开探究,请你参与。
[探究活动一]证明变质的样品仍然有氢氧化钠存在
资料摘要:碳酸钠的水溶液呈碱性,氯化钠、氯化钙的水溶液呈中性。
(1)氢氧化钠暴露在空气中发生变质反应的化学方程式为 。
同学们按照如下所示的步骤进行实验:
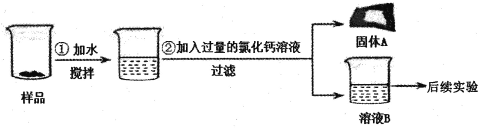
(2)步骤②中加入过量的氯化钙溶液的目的是 ;固体A必定含有的物质是 (写化学式)。
(3)“后续实验”验证氢氧化钠的存在,请你简述实验步骤和产生的现象: 。
[探究活动二]测定样品中碳酸钠的质量分数
取5.3g样品与足量的稀硫酸反应,测量生成二氧化碳的体积,从而计算出碳酸钠的质量分数。实验装置如图(不考虑其他因素的影响,装置的气密性良好):
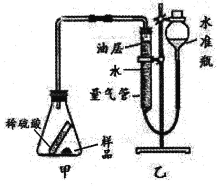
(4)倾斜锥形瓶使样品与稀硫酸充分接触。写出甲装置中发生反应的一个化学方程式: 。
(5)量气管中水面上要加一层植物油(二氧化碳不溶于该油层),目的是 。
(6)实验测得的部分数据如下表所示:
反应前 | 反应后 | |
量气管内液面对应的刻度 | 42mL | 262mL |
根据表中的实验数据计算,反应生成的二氧化碳体积为 mL,已知在实验条件下,二氧化碳的密度为2g·L-1,则生成二氧化碳的质量为 g。
(7)通过计算,样品中碳酸钠的质量分数为 。