题目内容
(一)下图是实验室制取气体的部分装置,请根据实验装置(部分固定装置已省略)回答问题:
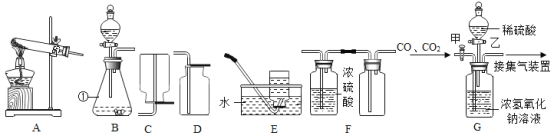
(1)图中标识①仪器的名称是:__________;
(2)实验室既可以制取CO2,又可以制取O2的发生和收集装置组合为:_______;(在A—E中选)
(3)若用F装置收集一瓶干燥的某气体,则该气体可能是_____;(填字母代号)
A.O2 B.NH3 C.H2 D.CO2
(4)如 B 装置分液漏斗改为长颈漏斗并增加多孔塑料板来制取二氧化碳,其优点为:_______。
(5)工业上常需分离CO、CO2的混合气体。某同学采用装置G也能达到分离该混合气体的目的,操作步骤如下:
①关闭活塞乙,打开活塞甲,通入混合气体,可收集到_____气体;
②然后,______填操作),又可收集到另一种气体。
(二)小红和她的同学学习了稀硫酸的一些性质后,对铜与浓硫酸能否发生反应产生了兴趣,并进行了如下探究:
(提出问题)猜想Ⅰ:铜与浓硫酸不能反应;
猜想Ⅱ:铜与浓硫酸能反应,且可能生成氢气。
(实验探究)实验Ⅰ:在一支试管中加入一小片铜,再加入少量的浓硫酸,放置一段时间,试管中无现象;
实验Ⅱ:再给上述试管加热,试管中产生有刺激性气味的气体,将反应后的溶液小心地注入到盛有少量水的烧杯中,溶液呈现出明显的蓝色。
(分析猜想)①溶液呈蓝色,说明生成了 _______________(填化学式)。
②根据实验现象及已有的知识推断,产生的气体不可能是氢气,很可能是一种含硫元素的气体。
(查阅资料)①常见的含硫元素的气体有二氧化硫和硫化氢。
②二氧化硫和二氧化碳相似,都能和氢氧化钠等碱溶液反应生成盐和水。
③二氧化硫能使品红溶液褪色,加热,又能恢复原来的红色。硫化氢不能使品红溶液褪色。
④二氧化硫和硫化氢均有毒。
(实验探究)为了检验产生的有刺激性气味的气体的成分,小红和她的同学进一步实验: 将产生的气体通入品红溶液中,品红溶液褪色,加热,溶液又恢复了红色。
(实验结论)①在常温下,铜与浓硫酸不能反应
②在加热条件下铜与浓硫酸反应产生的气体是_____(填化学式),此反应还生成了水,请写出该反应的化学方程式_____;
③浓硫酸与铜加热时能反应,而稀硫酸与铜即使加热也不能反应,由此说明:物质的化学性质除了与物质本身的性质有关外,还可能与溶液中溶质的_____有关。
(拓展延伸)为了防止污染空气,小红和她的同学采用氢氧化钠溶液来吸收多余的气体, 请写出该反应的化学方程式_____。
 阅读快车系列答案
阅读快车系列答案

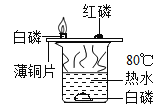 燃烧条件探究
燃烧条件探究 石蕊溶液变红
石蕊溶液变红 肥皂水区别硬水和软水
肥皂水区别硬水和软水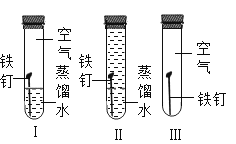 铁钉绣蚀
铁钉绣蚀
 4X+C2H4,则X的化学式为_____。
4X+C2H4,则X的化学式为_____。