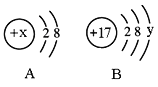��Ŀ����
����Ŀ������ͼ��ԭ������Ϊ1��18��Ԫ�ص�ԭ�ӽṹʾ��ͼ������ͼ����Ϣ�ش����⡣
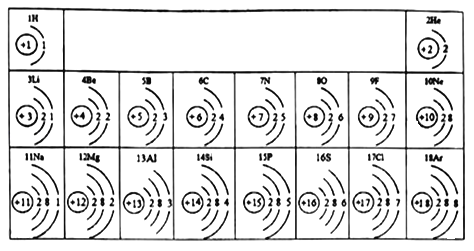
��1��þ�������ڲ�ͬ��Ԫ�أ�����Ϊ����Ԫ�ص�ԭ����_____��ͬ��ԭ������Ϊ11��17������Ԫ���γɵĻ�������_____������ӡ�����ԭ�ӡ������ӡ������ɣ��仯ѧʽΪ_____
��2��ԭ������Ϊ12��ԭ���ڻ�ѧ��Ӧ������_____����õ�����ʧȥ�������ӣ��γ�_____�������������������
��3��д��ԭ������Ϊ1��Ԫ���γɵĵ�����ԭ������Ϊ17��Ԫ���γɵĵ�����ȼ�յĻ�ѧ����ʽ_��
���𰸡� ������ ���� NaCl ʧȥ �� H2+Cl2![]() 2HCl
2HCl
����������1����ͬ��Ԫ�صı���������ԭ���е���������ͬ��ԭ������Ϊ11��17������Ԫ���γɵĻ�������NaCl��NaCl�����ӹ��ɡ���2��ԭ������Ϊ12��ԭ�ӣ��������2�����ӣ��ڻ�ѧ��Ӧ������ʧȥ2�����ӣ���������λ������ɣ��γ������ӡ���3��ԭ������Ϊ1��Ԫ���γɵĵ�����������ԭ������Ϊ17��Ԫ���γɵĵ�����������������������ȼ�յĻ�ѧ����ʽΪ��H2+Cl2![]() 2HCl
2HCl

����Ŀ��ͬѧ�Ǵ�ɽ�ϲɼ���һ��ʯ��ʯ������ȡ80 g����Ʒ��������ʵ�飨�������������չ����в������仯������÷�Ӧ������������m���뷴Ӧʱ�䣨t���Ĺ�ϵ�����
��Ӧʱ��t�Ms | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
��Ӧ����������m�Mg | 80 | 75 | 70 | 66 | 62 | 58 | 58 |
��ش��������⣺
��1����ʯ��ʯ��ȫ��Ӧ������CO2��������
��2�����ʯ��ʯ��CaCO3������������д��������̣�
��3��������ͼ��ʾ������ͼ�У���������ʱ���������������m����ʱ�䣨t���仯�����ߣ�