题目内容
【题目】化学用语是学习化学的重要工具。
(1)人们常说:①高原缺氧 ②生理盐水 ③胃酸过多 ④发酵粉中的小苏打。请用化学符号表示:
①中的“氧”_______;②中的“盐”________;③中的“酸”________;④中的“小苏打”_______。
(2)下图是几种常见的清洁剂,请按要求写出相应的化学方程式:

①“彩漂液”的有效成分为过氧化氢,长期存放会因分解而失效:_________________;
②“洁厕灵”的有效成分为盐酸,不小心滴到大理石地面上,发现有气泡产生:______________;
③“管道通”的有效成分为氢氧化钠,它不能与“洁厕灵”混合使用,其原因是:__________;
④ “84消毒液”的有效成分为次氯酸钠(NaClO),与“洁厕灵”混合使用会产生有毒气体氯气(Cl2),以及氯化钠溶液:________________________。
【答案】![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
过氧化氢分解生成水和氧气,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,氢氧化钠和盐酸反应生成氯化钠和水。
(1)①中的“氧”是指氧气,化学式为![]() 。
。
②中的“盐”是指氯化钠,化学式为![]() 。
。
③中的“酸”是指盐酸,化学式为![]() 。
。
④中的“小苏打”是指碳酸氢钠,化学式为![]() 。
。
①“彩漂液”的有效成分为过氧化氢,长期存放会因分解而失效,是因为过氧化氢分解生成水和氧气,反应的化学方程式为![]() 。
。
②“洁厕灵”的有效成分为盐酸,不小心滴到大理石地面上,发现有气泡产生,是因为碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为![]() 。
。
③“管道通”的有效成分为氢氧化钠,它不能与“洁厕灵”混合使用,其原因是氢氧化钠和盐酸反应生成氯化钠和水,反应的化学方程式为![]() 。
。
④“84消毒液”的有效成分为次氯酸钠(NaClO),与“洁厕灵”混合使用会产生有毒气体氯气(
![]() ),以及氯化钠溶液,反应的化学方程式为
),以及氯化钠溶液,反应的化学方程式为![]() 。
。

【题目】在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂。他们对该试剂进行了定量实验称取试剂19.8 g放入锥形瓶中,加入30.2 g的水,充分振荡,再向锥形瓶中依次滴加25 g盐酸充分反应。测得部分数据与图像如下。请根据有关信息回答问题。
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
加入盐酸的质量/g | 25 | 25 | 25 | 25 | 25 | 25 |
锥形瓶中物质的质量/g | 75 | 100 | a | 150 | 172.8 | 197.8 |
(1)a的数值为__________,兴趣小组的同学通过实验,得出该试剂已部分变质的结论,其依据是(通过实验数据和图像写出你的分析) _______________________________。
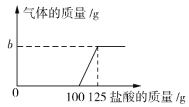
(2)b的数值为____________。
(3)计算该试剂中氢氧化钙的质量分数___________(写出计算过程,结果保留一位小数)。
【题目】某化学兴趣小组提出可以用废锌渣(主要成分是ZnO、FeO、Fe2O3、CuO)进行适当处理可制得硫酸锌晶体(ZnSO4·x H2O)。
Ⅰ、硫酸锌晶体的制备
该兴趣小组同学设计了如下流程:

已知:①硫酸锌晶体难溶于酒精
②硫酸锌晶体受热易逐步失去结晶水
③几种物质沉淀时的pH如下表:
物质 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
开始沉淀时pH | 1.48 | 6.2 | 5.2 |
完全沉淀时pH | 3.2 | 8.0 | 6.4 |
(1)酸浸中生成硫酸锌的化学方程式为___________,属于________(填基本类型)反应。
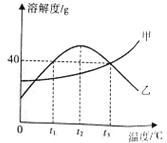
(2)酸浸时温度和时间对锌浸出率的影响见下图。为了提高锌的浸出率,反应的最佳温度是__________℃,最佳时间是____________min;
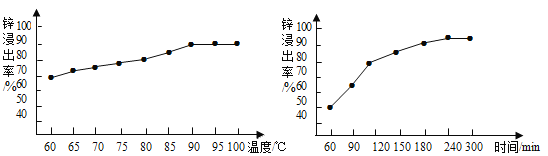
(3)加H2O2的目的是将酸浸后的Fe2+氧化成Fe3+,其反应方程式为2FeSO4 + H2O2 + _____= Fe2(SO4)3 + 2H2O,KMnO4溶液也能将Fe2+氧化成Fe3+,并生成可溶性的锰盐,选择H2O2的优点是_________;
(4)加入ZnO调节溶液的pH约为4的目的是__________;
(5)流程中,滤渣Y的成分为_________________;
(6)流程中“一系列操作”主要过程为:①_________________ 、冷却结晶、过滤,加入酒精洗涤,重复几次,最后低温烘干,得到ZnSO4·xH2O;
②用酒精洗涤的目的是洗去晶体表面的杂质、避免因水洗涤所造成的晶体损耗、_________;
③低温烘干的原因是_______________。
Ⅱ、硫酸锌晶体(ZnSO4·xH2O)组成的测定
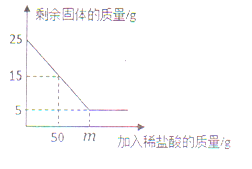
学习小组取5.74g硫酸锌晶体(ZnSO4·xH2O)进行加热分解,获得相关数据,并绘制成剩余固体质量一温度的关系图。
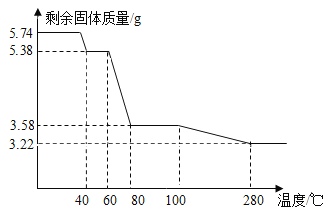
(7)280℃时,固体完全失去结晶水。根据图中数据,计算ZnSO4·xH2O中x的值为_____________;(请写出计算过程)
(8)加热过程中,硫酸锌晶体分步失去结晶水。请写出60℃到80℃时反应方程式_________。
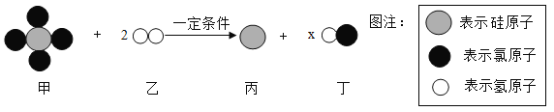
【题目】在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中钠在其中继续燃烧,反应后冷却,瓶底附着有黑色颗粒,同时瓶壁上粘附着白色物质.老师告诉甲同学瓶底附着黑色颗粒是碳单质,但没有告诉瓶壁上粘附着白色物质是什么,让同学们继续探究.
(进行猜想)甲同学认为:白色物质可能是Na2O或Na2CO3
乙同学认为:白色物质可能是NaOH
甲同学立刻认为乙同学的猜想是错误的,其理由是_____.
(查阅资料)氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O═2NaOH
(实验探究)甲同学对白色物质进行实验探究.
实验方案 | 实 验 操 作 | 实验现象 | 结 论 |
方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质 为Na2O |
方案2 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入适量_____溶液 | _____ | 白色物质 是Na2CO3 |
(反思评价)丙同学认为方案1得到的结论不正确,理由是_____.
(得出结论)钠在二氧化碳中燃烧的化学方程式为_____.
通过以上探究,你对燃烧和灭火有什么新的认识,请写出一点._____.