题目内容
【题目】A~H为初中化学常见物质。其中A、E为氧化物且E为常见的液体,B、D为碱,H、G为单质:C为石灰石的主要成分,F为胃酸的主要成分:反应①为光合作用。它们之间的相互关系如下图所示,其中“→”表示转化关系,“一”表示相互之间能发生反应(部分反应物、生成物以及反应条件省略)。
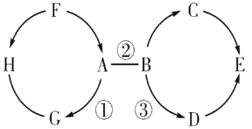
请回答下列问题:
(1)D的化学式为_______,H的化学式为_____。
(2)A与B反应的化学方程式为_______。
(3)C生成E的实验现象是______。
【答案】NaOH H2 CO2+Ca(OH)2=CaCO3↓+H2O 白色固体逐渐减少(或减少至消失),固体表面有气泡产生
【解析】
C为石灰石的主要成分,F为胃酸的主要成分,所以C是碳酸钙,F是稀盐酸;稀盐酸能转化成A,且反应①为光合作用,所以A是二氧化碳,G为光合作用生成的氧气单质;H是能与氧气反应,通过稀盐酸转化的单质,所以H是氢气;B是能与二氧化碳反应的碱,且能转化成C碳酸钙,所以B是氢氧化钙;氢氧化钙和碳酸钠反应生成氢氧化钠和碳酸钙,氢氧化钠和盐酸反应生成水和氯化钠,所以D是氢氧化钠,E是水,代入检验,符合题意。
(1)D是氢氧化钠,H是氢气;故填:NaOH;H2;
(2)A与B反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;故填:CO2+Ca(OH)2=CaCO3↓+H2O;
(3)C生成E是碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,实验现象是白色固体逐渐减少(或减少至消失),固体表面有气泡产生。故填:白色固体逐渐减少(或减少至消失),固体表面有气泡产生。

 名校课堂系列答案
名校课堂系列答案【题目】为测定某样品中锌的质量分数,取10g此样品,分五次向其中加入稀硫酸使之充分反应(假设锌的样品中杂质不与稀硫酸反应,且不溶于水),每次加入的稀硫酸质量及测定剩余固体的质量,记录数据如下表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀硫酸的质量/g | 10 | 10 | 10 | 10 | 10 |
剩余固体质量/g | 8.4 | 6.8 | 5.2 | 3.6 | 3.6 |
请认真分析表中的数据,回答下列问题:
(1)表示样品与稀硫酸恰好完全反应的是上表中第________次操作;
(2)计算样品中锌的质量分数; ____
(3)计算实验中所用稀硫酸的溶质质量分数。 ______