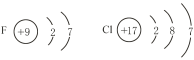题目内容
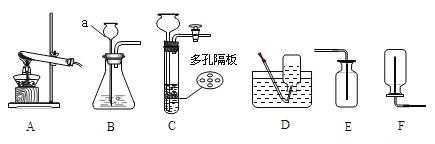
【题目】(10分)如图是实验室制取气体的部分装置.
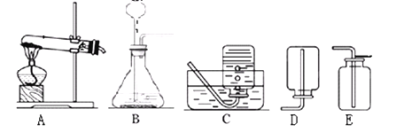
(1)在用上面的两套装置制取气体前,我们首先要检查装置的 ;
(2)选用A装置加热高锰酸钾制取氧气,该反应的化学方程式为 ____________;
(3)选用B装置制取一瓶干燥的氧气,应选择的收集装置是 (填字母),写出用该方法制取氧气的化学方程式 。
【答案】(1)气密性(2)2KMnO4![]() K2MnO4+MnO2+O2↑(3)E 2H2O2
K2MnO4+MnO2+O2↑(3)E 2H2O2 ![]() 2H2O +O2↑
2H2O +O2↑
【解析】
试题分析:制取气体前,我们首先要检查装置的气密性,防止漏气,加热高锰酸钾制取氧气,该反应的化学方程式为2KMnO4![]() K2MnO4+MnO2+O2↑,注意标注气体符号和配平方程式。制取一瓶干燥的氧气,应选择的收集装置是向上排气法,因为氧气的密度大于空气的密度,用B装置制取一瓶氧气,没有加热的条件,所以选用的药品时过氧化氢溶液。
K2MnO4+MnO2+O2↑,注意标注气体符号和配平方程式。制取一瓶干燥的氧气,应选择的收集装置是向上排气法,因为氧气的密度大于空气的密度,用B装置制取一瓶氧气,没有加热的条件,所以选用的药品时过氧化氢溶液。

 阅读快车系列答案
阅读快车系列答案【题目】(9分)某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
(1)为探究催化剂的种类对双氧水分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g 10%H2O2溶液与1.0g MnO2均匀混合
Ⅱ.将x g 10%H2O2溶液与1.0g CuO均匀混合
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是 。
Ⅱ中x的值应为 。
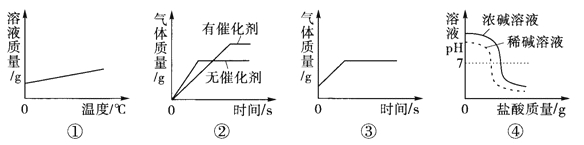
(2)乙探究了影响双氧水分解速度的某种因素.实验数据记录如下:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9mL |
Ⅱ | 50.0g | 2% | 0.1g | 16mL |
Ⅲ | 50.0g | 4% | 0.1g | 31mL |
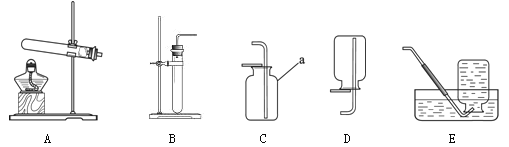
本实验中,测量O2体积的装置是 (填编号)
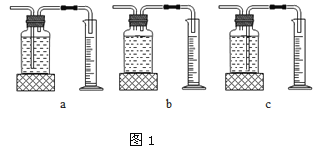
实验结论:在相同条件下, ,双氧水分解得越快。
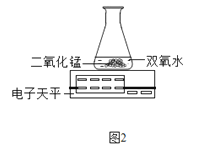
(3)丙用如图2装置进行实验,通过比较 也能达到实验目的。
【题目】关于下列事实的解释不正确的是
选项 | 事实 | 解释 |
A | 10mL酒精和10mL 水混合后体积小于20mL | 分子之间有间隔 |
B | 金刚石和石墨都由碳元素组成,物理性质有较大差异 | 碳原子的排列不同 |
C |
F 、Cl原子化学性质相似 | 化学反应中都易得到1个电子 |
D | 不能用铁制容器配制农药波尔多液(硫酸铜溶液和氢氧化钙按一比例混合) | 铁制容器能加速氢氧化钙与空气中二氧化碳的反应 |