题目内容
【题目】工业上采用如图的流程从海水中提取精盐:
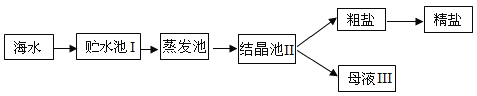
(1)上述流程中Ⅰ、Ⅱ、Ⅲ中对氯化钠来说溶液的状态分别是____、___、___。(填“饱和”或“不饱和”)
(2)从海水中提取粗盐的过程中,利用了___的方法,得到粗盐。
【答案】不饱和 饱和 饱和 蒸发结晶
【解析】
(1)将海水引入到贮水池Ⅰ,海水的成分基本不变,此时是氯化钠的不饱和溶液。随后进行蒸发结晶,得到结晶池Ⅱ,该过程中有晶体析出,所以此时的溶液一定是氯化钠的饱和溶液。之后经过过滤,得到粗盐和母液Ⅲ,母液由结晶池过滤而得,所以母液也一定是氯化钠的饱和溶液。故答案为:不饱和、饱和、饱和;
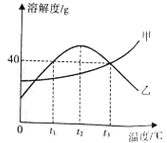
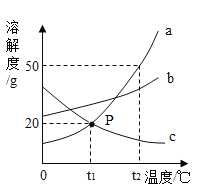
(2)从海水提取粗盐的过程中,本质是将氯化钠溶液中的晶体析出。氯化钠的溶解度随温度的升高而增大但是变化不明显,所以适合使用蒸发结晶的方法析出晶体。故答案为:蒸发结晶。

 全能测控一本好卷系列答案
全能测控一本好卷系列答案【题目】制笔行业中经常用到铂、钌(Ru)等贵金属。现有 5 种含钌元素的物质:Ru、RuO2、Ru2O3、RuCl3、K2RuO4。回答下列问题:
(1)RuO2 读作__________。
(2)上述 5 种物质中钌元素的化合价一共有_________种。
(3)从物质分类角度来看,K2RuO4 属于_________。(填选项)
A.化合物 | B.氧化物 | C.碱 | D.盐 |
(4)H2 与 Ru2O3 在加热条件下反应可得到 Ru。写出反应的化学方程式 。
【题目】某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖.对于该溶液是否变质,同学们开始实验探究并设计如下实验.请你将实验设计补充完整.
【猜想假设】
猜想(1):该溶液没有变质,为NaOH溶液.
猜想(2):该溶液全部变质,为 溶液.
猜想(3):该溶液部分变质,为NaOH和Na2CO3的混合溶液.
【查阅资料】Na2CO3溶液呈碱性,氯化钙溶液呈中性.
【设计方案】请你完善下表几组同学探讨的设计方案
实验操作 | 可能出现的现象与结论 | 同学评价 | |
第1组 |
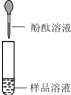
| 若溶液变红,则猜想(2)不成立 | 第2组同学认为:此方案结论不正确,理由是: . |
第2组 |
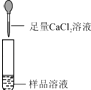
| 若产生白色沉淀,反应方程式是: 则猜想(1)不成立. | 第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立. |
第3组 |
| 若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立. | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:
|
【探究实验】综合各小组的方案后,动手实验.
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存.
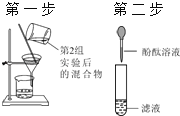
【拓展延伸】同学们设计了下列两套装置进行实验:
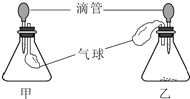
用胶头滴管吸取某种液体,锥形瓶中充入一种气体或放入一种固体物质,挤压胶头滴管.一段时间后,两装置中气球明显胀大.
(1)甲装置中可能发生反应的方程式是 .
(2)若乙装置中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是 .