题目内容
【题目】为了测定某赤铁矿石中氧化铁的质量分数,取矿石样品40g,加入盐酸,恰好完全反应时,共用去盐酸219g,过滤、洗涤、干燥后得滤渣8g(矿石中的杂质既不溶于水也不与盐酸反应)。计算:
(1) 赤铁矿石中氧化铁的质量分数; _________
(2)盐酸的溶质质量分数 _________
【答案】80% 20%
【解析】
稀盐酸和氧化铁反应生成氯化铁和水。
(1) 取矿石样品40g,加入盐酸,恰好完全反应时,共用去盐酸219g,过滤、洗涤、干燥后得滤渣8g,则氧化铁的质量为![]() ,故赤铁矿石中氧化铁的质量分数为
,故赤铁矿石中氧化铁的质量分数为
![]()
(2)设盐酸中溶质的质量为x
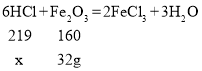
![]()
![]()
故盐酸的质量分数为:![]()
答:赤铁矿石中氧化铁的质量分数80%,盐酸的质量分数为20%。

 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案【题目】CaO和NaOH固体的混合物,俗称“碱石灰”,实验室常用作干燥剂。碱石灰在空气中容易吸收空气中的水和二氧化碳变质。某实验小组为确定一瓶久置的碱石灰样品的成分,设计了如图所示的实验流程;
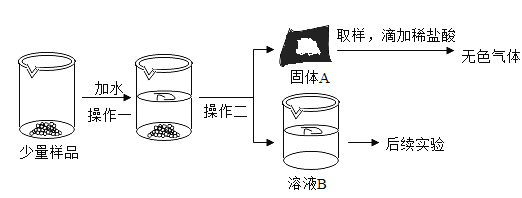
请你参与探究过程:
(1)固体A中一定含有_________。
(2)溶液B成分的探究:
(查阅资料)①Ca(OH)2、Na2CO3溶于水无明显的温度变化;② CaCl2溶液呈中性。
(猜想)溶液B中溶质可能为:①NaOH ②Na2CO3 ③NaOH和Na2CO3 ④Ca(OH)2和______(填化学式)。
(设计方案并进行实验)甲、乙同学分别设计如下方案并进行探究:
甲同学:取少量溶液B于试管中,滴加足量的稀盐酸,产生大量气泡,则溶液B中的溶质是Na2CO3;
乙同学:取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,则溶液B中的溶质一定含有NaOH。
(反思与评价)丙同学认真分析上述两位同学的实验,认为他们的结论均有不足之处,乙同学实验不足之处在于______________________________________。
为进一步确认溶液B中是否含NaOH,他做了如下实验:
实验步骤 | 实验现象 | 实验结论 |
①取少量溶液B于试管中,加入足量的________溶液 ②过滤,在滤液中滴加酚酞试液 | ①生白色沉淀 ②_______ | 猜想③正确 |
(3)实验过程中,同学们发现向样品中加水时还放出大量的热。综合以上探究,下列对样品成分分析正确的是______(填序号)。
A 一定有CaCO3 B 一定有NaOH C 一定有Na2CO3 D 可能有CaO