题目内容
【题目】元素周期表中磷元素的相关信息如图,下列说法不正确的是
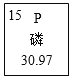
A. 磷元素的原子序数为15
B. 磷原子的质量为30.97g
C. 磷原子的结构示意图为
D. 一个磷原子中有15个质子
【答案】B
【解析】A.根据元素周期表中的一格中获取的信息,磷元素的原子序数为15,故A正确;B.根据元素周期表中的一格中获取的信息,可知磷元素的相对原子质量为30.97,相对原子质量单位是“1”,不是“克”,故B错误;C.磷元素的原子序数为15;根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为15,其原子结构未意图正确,故C正确;D.磷元素的原子序数为15;根据原子序数=核电荷数=质子数=核外电子数,则磷原子的原子核内有15个质子,故D正确;答案为B。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案【题目】以电石渣[主要成分Ca(OH)2和CaCO3]为原料制备KClO3的流程如图。
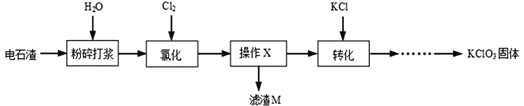
查阅资料:在75℃左右,氯化步骤中氯气转化成Ca(ClO3)2时发生一系列的反应,其中Cl2与Ca(OH)2反应的总化学方程式可表示为:
6 Ca(OH)2 + 6 Cl2 = Ca(ClO3)2 + 5CaCl2 + aH2O
(1)氯化前,先将电石渣粉碎的目的是___________。
(2)氯化步骤中所得产物氯酸钙Ca(ClO3)2中Cl的化合价为_______________价,a数值为___________。
(3)操作X为______________。转化步骤中Ca(ClO3)2与KCl反应生成KClO3的化学方程式为_____________。(相关物质的溶解度见下图)
物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
T℃时溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(4)对滤渣M的成分进行探究
【提出问题】滤渣M中除了电石渣原有的不溶性杂质外,还含有什么物质?
【猜想假设】①CaCO3; ②Ca(OH)2; ③___________。
【实验验证】
实验步骤 | 实验现象 | 结论 |
步骤1:取少量滤渣M加入盛水的小烧杯中,搅拌,静置后先加入_______; | 观察到___________现象 | 猜想①不正确 |
步骤2:向小烧杯中继续加入足量的稀盐酸 | 观察到___________现象 | 猜想③正确 |
