题目内容
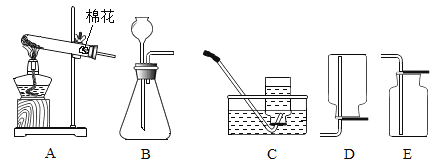
【题目】小明同学欲测定某纯碱样品(含少量氯化钠)中碳酸钠的质量分数,取26.5g该纯碱样品加入到100g水中,使其完全溶解,再加入169.3g稀盐酸,恰好完全反应,得到287g不饱和溶液。请计算:
(1)纯碱样品中碳酸钠的质量分数
(2)反应后得到的不饱和溶液中溶质的质量分数。
【答案】(1)80%;(2)10%
【解析】
(1)根据中质量守恒定律可以求算出生成二氧化碳的质量;利用二氧化碳的质量,然后结合反应的化学方程式可以列出样品中求算碳酸钠的比例式;进而求算出碳酸钠的纯度;
(2)反应后的溶液为氯化钠溶液,求出氯化钠的质量,进一步求解所得溶液中溶质质量分数。
(1)二氧化碳的质量为:100g+26.5g+169.3g﹣287g=8.8g;
设样品中碳酸钠质量为x,生成氯化钠的质量为y。
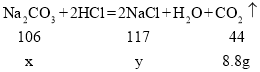
![]()
x=21.2g y=23.4g
所以该样品中碳酸钠的质量分数为![]() ;
;
(2)反应溶液中氯化钠的质量为:26.5g﹣21.2g+23.4g=28.7g
所得溶液中溶质质量分数为![]()
答:(1)样品中碳酸钠的纯度为80%;(2)所得溶液中溶质质量分数为10%。

练习册系列答案
相关题目
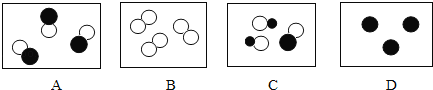
【题目】A在B中充分燃烧生成C和D,A、B、C、D的微观示意图如下图所示。
物质 | A | B | C | D |
|
分子示意图 |
|
|
|
|
看图回答:
(1)A、B、C、D中属于氧化物的是_____。
(2)A中氮、氢原子个数之比为_____,氮、氢元素质量之比为_____。
(3)A在B中充分燃烧的化学方程式为_____。