题目内容
【题目】硼及其化合物在工业上有很多用途。
(1)硼氢化钠(NaBH4)具有优良的还原性,在化学领域有着广泛的应用。利用硼精矿(主要成分为B2O3,含有少量Al2O3、SiO2、FeCl3等)制取NaBH4的流程如下图。

已知:(1)B2O3+2NaOH=2NaBO2+H2O;
(2)偏硼酸钠(NaBO2)易溶于水,不溶于醇,在碱性条件下稳定存在;
(3)Al2O3、SiO2均可与NaOH溶液反应生成可溶性钠盐。
回答下列问题:
(1)①操作1是_____________,滤渣主要成分为_____________(填化学式)。
②写出加快硼精矿溶解速率的措施______________(写一种)。
③MgH2中氢元素的化合价是____________
(2)单质硼可用于生成具有优良抗冲击性能硼钢,以硼酸(H3BO3)和金属镁为原料可以制备单质硼(B)。
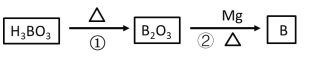
其制备过程先后通过两个化学反应,写出相关化学方程式:_______(属于置换反应)。
【答案】过滤 Fe(OH)3 将硼精矿粉碎、搅拌、增大NaOH浓度、升温等 -1 B2O3+3Mg![]() 3MgO+2B
3MgO+2B
【解析】
(1)①操作一将难溶性固体与液体进行了分离,该操作为过滤,故填过滤;
硼精矿中的氯化铁与氢氧化钠反应生成氢氧化铁沉淀和氯化钠,Al2O3、SiO2均可与NaOH溶液反应生成可溶性钠盐,偏硼酸钠(NaBO2)易溶于水,所以过滤后的滤渣的主要是氢氧化铁,其化学式为Fe(OH)3,故填Fe(OH)3。
②加快硼精矿溶解速率有将硼精矿粉碎、搅拌、增大NaOH浓度、升温等,故填将硼精矿粉碎或(搅拌或增大NaOH浓度或升温)等。
③镁元素的化合价为+2价,设氢元素的化合价为x,根据化合物中的各元素的化合价的代数和为零,则+2+x×2=0,x=-1,故填-1。
(2)属于置换反应的是反应②,该反应是三氧化二硼和镁在加热的条件下反应生成氧化镁和硼,故反应的化学方程式写为:B2O3+3Mg![]() 3MgO+2B
3MgO+2B
。

 阅读快车系列答案
阅读快车系列答案