题目内容
【题目】科学家发现天然气中主要成分甲(CH4)和水在一定条件下可以生成一氧化碳和氢气。该反应的化学方程式为____________________________;但是如果改变反应条件就能生成某有机物R和氢气,若将6.4g的R充分燃烧生成7.2gH2O和8.8gCO2,则R燃烧消耗氧气的质量与R中氧元素的质量比为__________。
【答案】CH4 + H2O CO+3H2 3:1
CO+3H2 3:1
【解析】
科学家发现天然气中主要成分甲(CH4)和水在一定条件下可以生成一氧化碳和氢气。该反应的化学方程式为CH4 + H2O CO+3H2;根据质量守恒定律可知,R中含碳元素的质量与8.8g二氧化碳中碳元素的质量相等,碳元素质量=
CO+3H2;根据质量守恒定律可知,R中含碳元素的质量与8.8g二氧化碳中碳元素的质量相等,碳元素质量=![]() ,R中含氢元素的质量与7.2g水中氢元素的质量相等,氢元素质量=
,R中含氢元素的质量与7.2g水中氢元素的质量相等,氢元素质量=![]() ;则R中含氧元素的质量为:6.4g-2.4g-0.8g=3.2g;参加反应的氧气的质量为:7.2+8.8g-6.4g=9.6g;
;则R中含氧元素的质量为:6.4g-2.4g-0.8g=3.2g;参加反应的氧气的质量为:7.2+8.8g-6.4g=9.6g;
R燃烧消耗氧气的质量与R中氧元素的质量比为:9.6g:3.2g=3:1。

练习册系列答案
相关题目
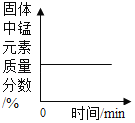
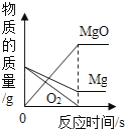
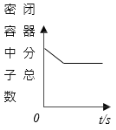
【题目】现有如图曲线,与之对应的叙述正确的是( )
|
|
|
|
A.加热一定质量的氯 酸钾和二氧化锰固 体混合物 | B.红磷在盛有空气 的密闭容器中燃 烧 | C.等质量的镁和氧 气充反应 | D.密闭容器中,氢气在足量的氧气中充 分燃烧 |
A.AB.BC.CD.D