题目内容
【题目】某同学用如图所示装置测定空气里氧气的含量,实验时,连接好装置并检查不漏气后再进行后续操作,下列说法正确的是
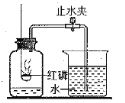
A.红磷燃烧时,要打开止水夹,以免瓶因温度升高,气压较大,造成橡皮塞从瓶口脱落
B.在空气里点燃红磷后,应缓慢把燃烧匙伸入瓶内并塞紧橡皮塞
C.所用红磷要过量,以保证集气瓶内空气里的氧气能充分反应
D.仍用本装置,只把红磷换成燃烧的木炭,能够更精确测定空气里氧气的含量
【答案】C
【解析】
A、红磷燃烧时,不能打开止水夹,防止集气瓶内的气体受热膨胀,从导管逸散到空气中,使结果偏大,故选项A不正确;
B、在空气里点燃红磷后,应立即把燃烧匙伸入瓶内并塞紧橡皮塞,防止集气瓶内的气体受热膨胀,从集气瓶口逸散到空气中,使结果偏大,故选项B不正确;
C、红磷过量,使集气瓶内空气里的氧气能充分反应,得出正确的结果,故选项C正确;
D、用本装置,把红磷换成燃烧的木炭,不能得出正确的结果,木条燃烧生成二氧化碳气体,瓶内压强变化不大,故选项D不正确。
故选:C。

【题目】化学课上同学们进行实验验证酸的性质。
I. 与指示剂作用。

(1)在白色点滴板孔穴1、3中加入紫色石蕊溶液,观察到溶液变_____色。
(2)将无色酚酞溶液滴加到孔穴2、4中,观察到孔穴4中溶液为无色,而孔穴2中溶液变为橙色。同学们猜想孔穴2中的异常现象与硫酸溶液的浓度过高有关,并通过以下实验证明该猜想正确:取少量上述橙色溶液于试管中,加水稀释,观察到的现象是_____。
II. 与铁锈反应。
实验 | 实验试剂 | 实验现象 |
1 | 锈蚀铁钉+10 mL 稀盐酸 | 生成无色气泡,铁锈较快消失,溶液颜色变黄。 |
2 | 锈蚀铁钉+10 mL 稀硫酸 | 生成无色气泡,铁锈减少速度缓慢,溶液颜色未变黄。 |
(提出问题)实验1、2现象不同的原因是什么?
(查阅资料)HCl在水中会解离出H+和Cl-,H2SO4在水中会解离出H+和SO42-。
(假设猜想)可能和溶液中阴离子不同有关。
(进行实验)
实验 | 实验试剂 | 实验现象 |
3 | 锈蚀铁钉+10 mL稀硫酸 + _A_ | 生成无色气泡,铁锈减少速度比实验2快,溶液颜色变黄。 |
4 | 锈蚀铁钉+10 mL稀盐酸 + Na2SO4 | 生成无色气泡,铁锈减少速度比实验1慢,溶液颜色变黄。 |
(解释和结论)
(3)铁锈(主要成分为Fe2O3)和盐酸反应的化学方程式是_____。
(4)实验1中产生的无色气体是_____。
(5)实验3中,物质A是_____。
(6)结合实验1~4,得出的结论是_____。
【题目】化学小组的同学们在探究“分子运动”时,设计了如下几组实验:
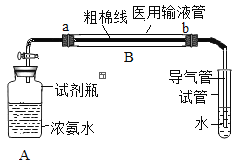
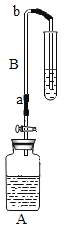
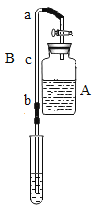
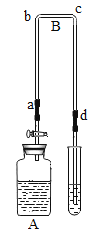
(实验装置)如图,实验1中的装置A取一个60 mL的试剂瓶,盖上一个单孔塞,单孔塞中插入一根带玻璃旋塞的导气管;装置B为一段医用输液管,内置一根浸泡过酚酞试剂并干燥的棉线。用橡胶管将A、B两装置链接。装置A 中加入约20 mL浓氨水,装置B的另一端连接导气管,导气管伸入小试管中。向小试管中加入一定量的蒸馏水。实验2、3、4的装置与实验1基本相同,只是根据实验需要变换了A、B装置和小试管的位置。
(实验步骤)①打开玻璃旋塞,观察现象。②将棉线润湿。
实验1 | 实验2 | 实验3 | 实验4 |
|
|
|
|
①干燥棉线没有明显变化。②湿润的棉线由a→b 逐渐匀速变红。 | 湿润的棉线由a→ b迅速变红,并且棉线变红的速率明显高于实验1 | 湿润的棉线由a→ b逐渐变红,并且棉线变红的速率明显低于实验1 装置。c→b 段棉线变红的速率比较缓慢,近b 端甚至不能变红。 | 湿润的棉线逐渐变红,并且a→b 段棉线变红的速率明显高于c→d 段棉线变红的速率 |
(1)以上实验得到的结论是:
①氨气不能使干燥的酚酞变色,氨气与水共同作用能够使酚酞试剂变红;
②_____;
③_____。
(2)若要应用实验1装置探究“温度对分子运动的影响”可以采取的操作是_____。