题目内容
对1~18 号元素的原子结构示意图按一定的规律排列如图: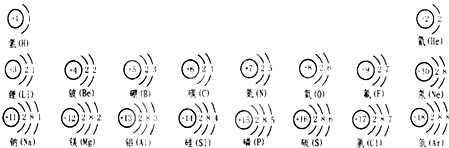
请你分析归纳:
(1)此表中每纵行原子的共同点是 ;
(2)此表中每横行原子的共同点是 ;
(3)第一纵行钠元素下的钾元素的原子结构示意图可能为 .
(4)核电荷数为12的原子电子层数为 ,在化学反应中易 电子变为 离子.

请你分析归纳:
(1)此表中每纵行原子的共同点是
(2)此表中每横行原子的共同点是
(3)第一纵行钠元素下的钾元素的原子结构示意图可能为
(4)核电荷数为12的原子电子层数为
考点:原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:由1--18 号元素的排列图可知:各元素的原子的最外层电子数、电子层数:
(1)通过观察纵行的原子的最外层的电子数得出纵行排列的依据;
(2)通过观察横行的原子的电子层数得出横行排列的依据;
(3)根据同一纵行的原子结构特点,由钠元素的原子结构推出钾元素的原子结构意图;
(4)本题要明确原子的结构示意图及其意义,圆圈内数字表示质子数,弧线表示电子层,弧线上数字表示电子数,根据原子核外最外层电子数,若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子.
(1)通过观察纵行的原子的最外层的电子数得出纵行排列的依据;
(2)通过观察横行的原子的电子层数得出横行排列的依据;
(3)根据同一纵行的原子结构特点,由钠元素的原子结构推出钾元素的原子结构意图;
(4)本题要明确原子的结构示意图及其意义,圆圈内数字表示质子数,弧线表示电子层,弧线上数字表示电子数,根据原子核外最外层电子数,若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子.
解答:解:(1)由表中的原子结构示意图可知,此表纵列排列的依据是最外层电子数相同;
(2)由表中的原子结构示意图可知,此表横行排列的依据是电子层数相同;
(3)根据氢、锂、钠的变化规律可知钾的原子结构示意图最外层电子数为1,一共有4层电子,故钾的原子结构示意图如右图
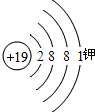
(4)由原子的结构示意图及其意义可知该元素原子的核电荷数为12,质子数为12为镁原子,核外有 3个电子层.最外层有2个电子,在化学反应中这种原子容易失去2个电子,变成阳离子,而成为稳定结构;
答案:
(1)最外层电子数相同;
(2)电子层数相同;
(3)
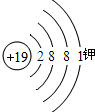
(4)3 失去 阳
(2)由表中的原子结构示意图可知,此表横行排列的依据是电子层数相同;
(3)根据氢、锂、钠的变化规律可知钾的原子结构示意图最外层电子数为1,一共有4层电子,故钾的原子结构示意图如右图

(4)由原子的结构示意图及其意义可知该元素原子的核电荷数为12,质子数为12为镁原子,核外有 3个电子层.最外层有2个电子,在化学反应中这种原子容易失去2个电子,变成阳离子,而成为稳定结构;
答案:
(1)最外层电子数相同;
(2)电子层数相同;
(3)

(4)3 失去 阳
点评:了解元素周期表的特点及其应用;核外电子在化学反应中的作用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
有三瓶无色无味气体,分别是氧气、空气、氮气,区分它们最简单的方法是( )
| A、测定气体的密度 |
| B、伸入燃着的木条 |
| C、滴入澄清的石灰水,振荡 |
| D、滴入紫色的石蕊溶液,振荡 |