题目内容
【题目】雨欣同学设计了如图实验装置验证一氧化碳的部分性质并验证产物.
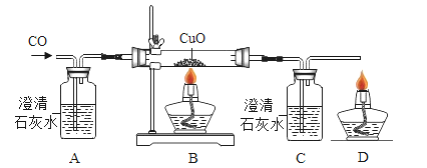
(1)实验时,在点燃B处酒精灯之前先通一段时间一氧化碳的目的是________,实验过程中B处玻璃管中的现象是________
(2)C中反应的化学方程式是 ________,D处点燃的目的是________
(3)对该实验的分析正确的是 ________ (填序号);
①实验结束时应先熄灭D处酒精灯
②C中增加的质量与B中固体减小的质量相等
③反应结束后,若生成了6.4g的铜,则通入的一氧化碳质量一定大于2.8g
(4)雨欣同学认为A装置用于证明一氧化碳不能和石灰水反应,有同学认为省略A可达到同样的目的,理由是________
【答案】把玻璃管中空气全部排出;黑色粉末变红Ca(OH)2+CO2═CaCO3↓+H2O;防止有毒的一氧化碳排放到空气中污染环境③为了排尽装置内的空气,反应前已经通入一段时间的CO
【解析】
(1)一氧化碳是易燃性气体,如混有氧气,温度达到一氧化碳的着火点的话,有可能急速燃烧,发生爆炸,故为了防止引起爆炸,需要先通入一段时间一氧化碳,把玻璃管中空气全部排出;B装置中是黑色的氧化铜与一氧化碳反应生成二氧化碳气体和红色的铜,故现象为黑色粉末变为红色。
(2)C装置中是氢氧化钙与二氧化碳反应生成碳酸钙和水,反应方程式为Ca(OH)2+CO2═CaCO3↓+H2O;该反应中一氧化碳是有毒的气体,为了防止一氧化碳排放到空气中污染空气,需要在D处用酒精灯点燃没有完全反应的一氧化碳。
(3)①实验结束时应先熄灭D处酒精灯实验结束时,为了防止B中的铜被再次氧化,需要继续通入一氧化碳至室温,故应该后熄灭D处的酒精灯,故错误;
②B装置中减少了氧元素的质量,而C中增加的质量是二氧化碳的质量,故不相等,故错误;
③设生成6.4g的铜可生成需要一氧化碳的质量为x
CuO + CO ![]() Cu + CO2
Cu + CO2
28 64
x 6.4g
![]() =
=![]()
x=2.8g,该实验前与实验结束后都要通入一氧化碳,故通入一氧化碳的质量一定大于2.8g。故③正确。故选③
(4). 实验开始前为了排尽装置内的空气,反应前已经通入一段时间的CO,一氧化碳已经与C中氢氧化钙进行了充分的接触,故不需要A装置;

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案【题目】某化学兴趣小组在学习催化剂的概念后,想研究不同的氧化物能否在氯酸钾制取氧气实验中起催化作用,进行了以下实验:
实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
1 | 0.6 | / | 9.8 | 480 |
2 | 0.6 | 0.2g二氧化锰 | 67 | 36.5 |
3 | 0.6 | 0.2g氧化铜 | 67 | 89.5 |
⑴写出实验2反应的化学方程式____________________。
⑵为证明氧化铜是该反应的催化剂,同学们又完成了以下的实验:
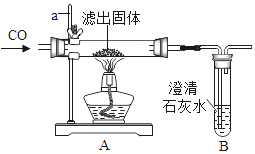
Ⅰ.在实验3反应后的混合物中加足量的水溶解,过滤,将滤渣洗涤并干燥,用电子天平称量,质量为0.2g。
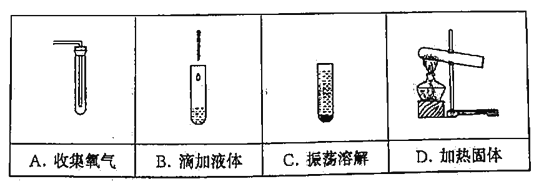
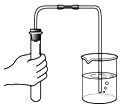
Ⅱ.将过量的CO通入滤出的固体,按如图进行实验:仪器a的名称_________________。
⑶甲同学的实验报告如下:
装置 | 现象 | 实验结论 |
A | 黑色固体全部变红 | 生成了铜,反应方程式________________ |
B | 石灰水变浑浊 | 产生了二氧化碳 |
Ⅲ.该实验装置存在的缺陷是______________;当出现______现象时,证明反应已经开始。
⑷以上实验证明氧化铜在反应前后质量和化学性质都没改变,能作为氯酸钾受热分解的催化剂。两种氧化物相比,________的催化效果更好。